题目内容
1.用NA表示伏伽德罗常数的值,下列说法错误的是( )| A. | 常温常压下28g氮气含有的原子数是2NA | |
| B. | 标准状况下,22.4L醋酸的水分子数是NA | |
| C. | 1molCl2与足量Fe反应,转移的电子数为2NA | |
| D. | 500mL 2mol•L-1Al(SO4)3溶液中SO42-的数目为3NA |
分析 A、求出氮气的物质的量,然后根据氮气是双原子分子来分析;
B、标况下,醋酸是液体;
C、根据反应后氯元素的价态为-1价来分析;
D、求出Al2(SO4)3的物质的量,然后根据1molAl2(SO4)3中含3molSO42-来计算.
解答 解:A、28g氮气的物质的量n=$\frac{28g}{28g/mol}$=1mol,而氮气是双原子分子,故1mol氮气中含2mol氮原子,即2NA个,故A正确;
B、标况下,醋酸是液体,故不能根据气体摩尔体积来计算物质的量,故B错误;
C、反应后氯元素的价态为-1价,故1mol氯气转移2mol电子,故C正确;
D、Al2(SO4)3的物质的量n=CV=2mol/L×0.5L=1mol,而1molAl2(SO4)3中含3molSO42-,即3NA个,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,应熟练掌握公式的运用和物质的状态,难度不大.

练习册系列答案
相关题目
12.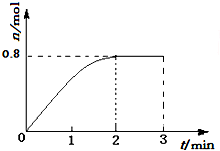 一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?C(g)+2D(s).2min末该反应达到平衡,生成D的物质的量如图.下列判断正确的是( )
一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?C(g)+2D(s).2min末该反应达到平衡,生成D的物质的量如图.下列判断正确的是( )
 一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?C(g)+2D(s).2min末该反应达到平衡,生成D的物质的量如图.下列判断正确的是( )
一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?C(g)+2D(s).2min末该反应达到平衡,生成D的物质的量如图.下列判断正确的是( )| A. | 若混合气体的密度不再改变时,该反应不一定达到平衡状态 | |
| B. | 2min后,加压会使正反应速率加快,逆反应速率变慢,平衡正向移动 | |
| C. | 反应过程中A和B的转化率之比为3:1 | |
| D. | 该条件下此反应的化学平衡常数的数值约为0.91 |
16.下列实验能获得成功的是( )
| A. | 苯和浓溴水用铁作催化剂制溴苯 | |
| B. | 氯乙烷与NaOH溶液共热,在水解后的溶液中直接加入AgNO3溶液检验Cl- | |
| C. | CH4与Cl2在光照条件下制备纯净的CH3Cl | |
| D. | 乙烯通入Br2的CCl4溶液中制备CH2Br-CH2Br |
17.下列有机物命名正确的是( )
| A. | 3,3-二甲基丁烷 | B. | 3-甲基-1-戊烯 | ||
| C. | 2,2-二甲基-1-戊烯 | D. | 3-甲基-2-乙基戊烷 |
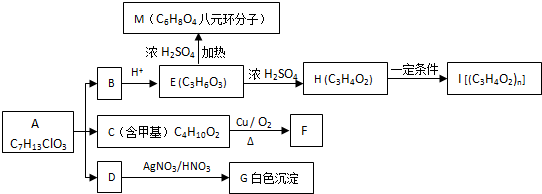

 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O;②E→M:2HOCH2CH2COOH $→_{△}^{浓H_{2}SO_{4}}$
+2H2O;②E→M:2HOCH2CH2COOH $→_{△}^{浓H_{2}SO_{4}}$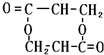 +2H2O;
+2H2O;