题目内容
1.恒温时,在一容积固定的容器中充入2mol的NO2,反应2NO2(g)?N2O4(g) 达到平衡时,向容器入通入2mol的NO2,重新达到平衡后,与第一次平衡时相比,NO2的转化率( )| A. | 不变 | B. | 增大 | C. | 减少 | D. | 无法确定 |
分析 固定容器中充入2mol的NO2,反应2NO2(g)?N2O4(g) 达到平衡时,向容器入通入2mol的NO2,等效为在原平衡的基础上压强增大一倍,平衡向正反应方向移动.
解答 解:固定容器中充入2mol的NO2,反应2NO2(g)?N2O4(g) 达到平衡时,向容器入通入2mol的NO2,等效为在原平衡的基础上压强增大一倍,平衡向气体体积减小的方向移动,即向正反应方向移动,重新达到平衡后,与第一次平衡时相比,NO2的转化率增大,故选B.
点评 本题考查等效平衡,侧重考查学生分析能力,注意利用等效思想构建平衡建立的途径,注意对等效平衡规律的理解掌握.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
16.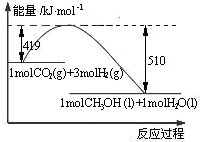 5、常温下,反应CO2(g)+3H2(g)?CH3OH(l)+H2O(l)的能量变化如图所示.反应达到平衡后,要使该反应化学平衡向右移动,其他条件不变,可采取的措施是( )
5、常温下,反应CO2(g)+3H2(g)?CH3OH(l)+H2O(l)的能量变化如图所示.反应达到平衡后,要使该反应化学平衡向右移动,其他条件不变,可采取的措施是( )
 5、常温下,反应CO2(g)+3H2(g)?CH3OH(l)+H2O(l)的能量变化如图所示.反应达到平衡后,要使该反应化学平衡向右移动,其他条件不变,可采取的措施是( )
5、常温下,反应CO2(g)+3H2(g)?CH3OH(l)+H2O(l)的能量变化如图所示.反应达到平衡后,要使该反应化学平衡向右移动,其他条件不变,可采取的措施是( )| A. | 升高温度 | B. | 分离出甲醇 | ||
| C. | 缩小反应器体积 | D. | 使用合适的催化剂 |
6.1mol钠、镁、铝分别与200mL2mol/L的盐酸反应,下列说法正确的是( )
| A. | 三种金属产生氢气的量相同 | |
| B. | 钠反应生成的氢气的量最多 | |
| C. | 铝反应产生的氢气的量最多 | |
| D. | 钠、镁与酸反应生成的氢气的量相同 |
13.下列配合物的配位数不是6的是( )
| A. | K2[Co(NCS)3]Cl | B. | Na2[SiF2Cl2Br2] | C. | Na3[AlF6] | D. | [Cr(NH3)4(H2O)2]Cl3 |
10.100g浓度为18mol/L密度为ρg/mL的浓硫酸中加入一定的水稀释成9mol/L的硫酸,则加入水的体积为( )
| A. | 小于100mL | B. | 等于100mL | C. | 大于100mL | D. | 等于100/ρmL |
11.已知16S和34Se位于同一主族,下列说法正确的是( )
| A. | 热稳定性:H2Se>H2S>H2O | B. | 原子半径:Se>Cl>S | ||
| C. | 酸性:H2SeO4<H2SO4<HClO4 | D. | 还原性:S2->Se2->Br- |
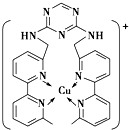 铜、碳、氮、硫、氯等是组成物质的重要元素.
铜、碳、氮、硫、氯等是组成物质的重要元素.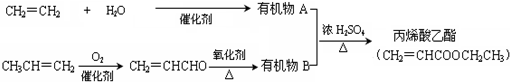
 ,反应类型是加聚反应.
,反应类型是加聚反应.