题目内容
17.下列各组物质中分类正确的是( )| 酸 | 碱 | 盐 | 氧化物 | |
| A | 硫酸 | 纯碱 | 石膏 | 碳酐 |
| B | 氢氯酸 | 烧碱 | 纯碱 | 生石灰 |
| C | 碳酸 | 明矾 | 胆矾 | 二氧化硫 |
| D | 二氧化碳 | 苛性钠 | 食盐 | 石灰石 |
| A. | A | B. | B | C. | C | D. | D |
分析 酸是能电离出的阳离子全部是H+的化合物;碱是电离出的阴离子全部是OH-离子的化合物;盐是电离出阳离子是金属阳离子或铵根离子、阴离子为酸根离子的化合物;氧化物由两种元素组成,其中一种为氧元素的化合物,根据相关概念解答该题.
解答 解:A、硫酸属于酸,纯碱是碳酸钠的俗称,属于盐类,石膏是硫酸钙的水合物,属于盐类,碳酸的酸酐是二氧化碳,属于氧化物,故A错误;
B、盐酸属于酸,烧碱是氢氧化钠的俗称,属于碱类,纯碱是碳酸钠的俗称,属于盐类,生石灰石氧化钙的俗称,属于氧化物,故B正确;
C、碳酸属于酸,明矾是硫酸铝钾的水合物,属于盐类,但凡是硫酸铜的晶体,属于盐类,二氧化硫属于氧化物,故C错误;
D、二氧化碳属于氧化物,氢氧化钠属于碱,食盐氯化钠属于盐类,石灰石是碳酸钙的俗称,属于盐类,故D错误.
故选B.
点评 本题考查酸碱盐以及氧化物的概念及分类,题目难度不大,解答本题的关键把握相关概念以及物质的组成和俗称.

练习册系列答案
相关题目
7.以碳化硅、氮化镓(GaN)等为代表的第三代半导体材料具有高发光效率、抗腐蚀、化学稳定性好、高强度等特性,是目前最先进的半导体材料.
(1)上述各种元素中,原子半径最小的元素原子的结构示意图是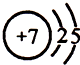 .
.
(2)碳化硅中的化学键类型是极性共价键.
(3)下列反应(或反应组)能说明碳的非金属性强于硅的是ac(选填编号).
a.SiO32-+2CO2+2H2O→H2SiO3+2HCO3-
b.SiO2+2C$\stackrel{高温}{→}$Si+2CO↑
c.SiH4$\stackrel{500℃}{→}$Si+2H2; CH4$\stackrel{>100℃}{→}$C+2H2
d.Si+O2$\stackrel{900℃}{→}$SiO2; C+O2$\stackrel{300℃}{→}$CO2
(4)镓、铝为同族元素,性质相似,现将一块镓铝合金完全溶于烧碱溶液中得到溶液X.已知:
①氢氧化镓的电离方程式是Ga3++3OH-?Ga(OH)3?GaO2-+H++H2O.
②镓与烧碱溶液反应的离子方程式是2Ga+2OH-+2H2O═2GaO2-+3H2↑.
③往X溶液中缓缓通入CO2,最先析出的氢氧化物是Al(OH)3.
(5)氮化镓(GaN)性质稳定,但能缓慢的溶解在热的NaOH溶液中.该反应的化学方程式是GaN+NaOH+H2O$\frac{\underline{\;\;△\;\;}}{\;}$NaGaO2+NH3↑.
(1)上述各种元素中,原子半径最小的元素原子的结构示意图是
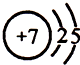 .
.(2)碳化硅中的化学键类型是极性共价键.
(3)下列反应(或反应组)能说明碳的非金属性强于硅的是ac(选填编号).
a.SiO32-+2CO2+2H2O→H2SiO3+2HCO3-
b.SiO2+2C$\stackrel{高温}{→}$Si+2CO↑
c.SiH4$\stackrel{500℃}{→}$Si+2H2; CH4$\stackrel{>100℃}{→}$C+2H2
d.Si+O2$\stackrel{900℃}{→}$SiO2; C+O2$\stackrel{300℃}{→}$CO2
(4)镓、铝为同族元素,性质相似,现将一块镓铝合金完全溶于烧碱溶液中得到溶液X.已知:
| Al(OH)3 | Ga(OH)3 | |
| 酸式电离常数Ka | 2×10-11 | 1×10-7 |
| 碱式电离常数Kb | 1.3×10-33 | 1.4×10-34 |
②镓与烧碱溶液反应的离子方程式是2Ga+2OH-+2H2O═2GaO2-+3H2↑.
③往X溶液中缓缓通入CO2,最先析出的氢氧化物是Al(OH)3.
(5)氮化镓(GaN)性质稳定,但能缓慢的溶解在热的NaOH溶液中.该反应的化学方程式是GaN+NaOH+H2O$\frac{\underline{\;\;△\;\;}}{\;}$NaGaO2+NH3↑.
8.下列叙述不正确的是( )
| A. | 将SO2通入BaCl2 溶液中至饱和,无沉淀产生,再通入Cl2,产生白色沉淀 | |
| B. | 纯锌与稀硫酸反应产生氢气速率较慢;再加入少量CuSO4 固体,速率不改变 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉可以溶解 | |
| D. | 向AlCl3 溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO4 溶液,沉淀消失 |
5.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1 mol ${\;}_{8}^{16}$OD-离子含有的质子、中子数均为10NA | |
| B. | 标准状况下,4.48 L己烷含有的分子数为0.2NA | |
| C. | 含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA | |
| D. | VL a mol•L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目等于3NA |
2.下列溶液中溶质的物质的量浓度为1mol•L-1的是( )
| A. | 将40g NaOH溶解于1L水中配成的NaOH溶液 | |
| B. | 常温常压下将22.4L HCl 气体溶于水配成1L的盐酸溶液 | |
| C. | 将100mL 10mol/L的浓盐酸加水900mL混合所配成的溶液 | |
| D. | 从1000mL 1mol/L NaCl溶液中取出100mL的溶液 |
9.分类是重要的化学学习方法.下列对应关系正确的是( )
| A. | 混合物--液氯、漂白粉 | B. | 碱性氧化物--Al2O3、Na2O2 | ||
| C. | 强电解质--NH4Cl、HClO | D. | 非电解质--NH3、SO2 |
6.下列说法正确的是( )
| A. | 一定温度下,向饱和NaOH溶液中加入一小块钠,充分反应后恢复到原来温度,溶液的pH不变,有氢气放出 | |
| B. | 已知钡的活动性处于钾和钠之间,则在溶液中钡离子可氧化金属锌,使之成为锌离子 | |
| C. | 研究小组通过实验探究Cu及其化合物的性质,将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色 | |
| D. | 次氯酸钠是漂粉精的主要成分 |
7.在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质,下列实验现象和结论一致且正确的是( )
| A. | 加入有色布条,有色布条褪色,说明溶液中有氯气分子存在 | |
| B. | 溶液呈现黄绿色,且有刺激性气味,说明有氯气分子存在 | |
| C. | 先加入盐酸酸化,再加入硝酸银溶液产生白色沉淀,说明有Cl-存在 | |
| D. | 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在 |
 ,F元素离子基态时的电子排布式1s22s22p63s23p6,E元素的原子结构示意图是
,F元素离子基态时的电子排布式1s22s22p63s23p6,E元素的原子结构示意图是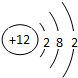 .
.