题目内容
2.下列溶液中溶质的物质的量浓度为1mol•L-1的是( )| A. | 将40g NaOH溶解于1L水中配成的NaOH溶液 | |
| B. | 常温常压下将22.4L HCl 气体溶于水配成1L的盐酸溶液 | |
| C. | 将100mL 10mol/L的浓盐酸加水900mL混合所配成的溶液 | |
| D. | 从1000mL 1mol/L NaCl溶液中取出100mL的溶液 |
分析 A、根据C=$\frac{\frac{m}{M}}{V}$中,体积指溶液体积不是溶剂体积;
B、根据温度、压强对气体摩尔体积的影响;
C、根据不同液体混合时体积能否直接加和判断;
D、根据溶液浓度的均一性判断.
解答 解:A.C=$\frac{\frac{m}{M}}{V}$中,体积指溶液体积不是溶剂体积,所以40gNaOH溶解于1L水中配成的NaOH溶液浓度不是1mol/L,故A错误;
B、气体摩尔体积受温度和压强的影响,温度越高,气体摩尔体积越大,标况下,22.4LHCl的物质的量是1mol,常温常压下,22.4LHCl的物质的量小于1mol,所以常温常压下将22.4LHCl气体溶于水配成1L的盐酸溶液的物质的量浓度不是1mol/L,故B错误;
C、将100mL 10mol/L的浓盐酸加水900mL混合所配成的溶液,溶液的体积不等于1000mL,所以混合后溶液的物质的量浓度不是1mol/L,故C错误;
D、溶液的物质的量浓度有均一性,与取出溶液的体积大小无关,从1000mL 1mol/L NaCl溶液中取出100mL的溶液,溶质浓度为1mol/L,故D正确;
故选D.
点评 本题考查了有关物质的量浓度的问题,难度不大,注意溶液的浓度有均一性,与取出溶液的体积大小无关.

练习册系列答案
相关题目
14.物质的分离与提纯是化学实验研究常用的方法.如表混合体系分离提纯对应的方法不正确的是( )
| 选项 | A | B | C | D |
| 混合体系 | 溴水 | 酒精与水 | 固体碘和氯化铵 | 混有少量KCl的KNO3粉末 |
| 分离方法 | 萃取、分液 | 加生石灰,蒸馏 | 加热 | 配成热的饱和溶液、降温结晶 |
| A. | A | B. | B | C. | C | D. | D |
11.下列物质在水溶液中的电离方程式不正确的是( )
| A. | Ca(OH)2═Ca2++2OH- | B. | Al2(SO4)3═2Al3++3SO42- | ||
| C. | NH4Cl═NH3+H++OH- | D. | HNO3═H++NO3- |

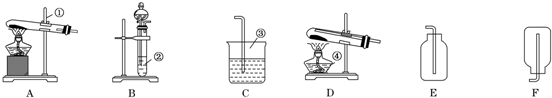
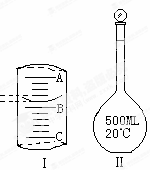 实验室配制500mL0.1mol•Lˉ1Na2CO3溶液,回答下列问题:
实验室配制500mL0.1mol•Lˉ1Na2CO3溶液,回答下列问题: