题目内容
如图所示实验合理的是( )
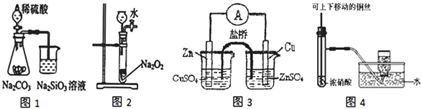

| A、图1证明非金属性强弱:S>C>Si |
| B、图2可制备少量氧气 |
| C、图3构成铜锌原电池,产生持续稳定的电流 |
| D、图4可制备并收集NO2气体 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.发生强酸制取弱酸的反应,可知酸性为硫酸>碳酸>硅酸;
B.过氧化钠为粉末固体,不能使反应随时停止;
C.左烧杯中发生化学反应,不能形成原电池;
D.二氧化氮与水反应.
B.过氧化钠为粉末固体,不能使反应随时停止;
C.左烧杯中发生化学反应,不能形成原电池;
D.二氧化氮与水反应.
解答:
解:A.发生强酸制取弱酸的反应,可知酸性为硫酸>碳酸>硅酸,则非金属性为S>C>Si,故A正确;
B.过氧化钠为粉末固体,不能使反应随时停止,则图中装置不能制备少量氧气,故B错误;
C.左烧杯中发生化学反应,不能形成原电池,则不能产生持续稳定的电流,故C错误;
D.二氧化氮与水反应,则图中排水法收集不合理,故D错误;
故选A.
B.过氧化钠为粉末固体,不能使反应随时停止,则图中装置不能制备少量氧气,故B错误;
C.左烧杯中发生化学反应,不能形成原电池,则不能产生持续稳定的电流,故C错误;
D.二氧化氮与水反应,则图中排水法收集不合理,故D错误;
故选A.
点评:本题考查化学实验方案的评价,为高频考点,把握物质的性质及化学反应原理为解答的关键,涉及酸性比较、气体的制备和收集及原电池等,注重高频考点的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
在酸性溶液中,可大量共存的离子是( )
| A、K+ Na+ OH- SO42- |
| B、Mg2+ SO42- NH4+ Cl- |
| C、K+ Na+ HCO3- Cl- |
| D、Ag+ Na+ NO3- Cl- |
下列离子方程式正确的是( )
| A、实验室中制取CO2:CO32-+2H+═CO2↑+H2O |
| B、钠投入CuSO4溶液中:2Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑ |
| C、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
| D、向酸性KMnO4溶液中滴加双氧水:2MnO4-+H2O2+6H+═2Mn2++3O2↑+4H2O |
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )


| A、X可能是一种氢化物 |
| B、M不可能是金属 |
| C、E可能是一种有色气体 |
| D、X→Y一定是非氧化还原反应 |
下列说法不正确的是( )
| A、利用分液漏斗进行分液操作时,先打开分液漏斗旋塞,使下层液体慢慢流出,待下层液体完全流出后,关闭旋塞,上层液体再从上面倒出 |
| B、固体药品取用:块状固体用镊子夹取,粉末状的用药匙或纸槽转移 |
| C、在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、环形玻璃搅拌棒进行搅拌、酸和过量的碱充分反应、取2-3次的实验平均值,以达到良好的实验效果 |
| D、用标准浓度的盐酸滴定未知浓度NaOH溶液时,酸式滴定管未用同浓度盐酸润洗,将导致测定结果偏低 |
将1mol冰醋酸加入到一定量的蒸馏水中最终得到1L溶液.下列各项中表征醋酸已达到电离平衡状态的是( )
| A、醋酸的浓度达到1mol?L-1 |
| B、H+的浓度达到0.5mol?L-1 |
| C、醋酸的浓度、醋酸根离子的浓度、H+的浓度均为0.5mol?L-1 |
| D、醋酸分子电离成离子的速率和离子重新结合成分子的速率相等 |
下列反应的离子方程式正确的是( )
| A、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ |
| B、氧化铝溶于氢氧化钠:Al2O3+2OH-═2AlO2-+H2↑ |
| C、硅酸钠溶液中滴加稀盐酸:SiO32-+2H+═H2SiO3↓ |
| D、将氨水滴入到FeCl3溶液中:Fe3++3OH-═Fe(OH)3↓ |
下列各组离子,在指定环境中能大量共存的是( )
| A、常温下,在PH>7的溶液中,Na+、S2-、K+、AlO2- |
| B、常温下,在PH>1的溶液中,SO32-、S2-、K+、NH4+ |
| C、常温下,在PH=1的溶液中,Fe2+、HCO3-、Na+、SO42- |
| D、常温下,在PH<7的溶液中,Fe3+、Cu2+、Cl-、NO3- |
下列各项表达式正确的是( )
A、S原子的结构示意图: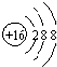 |
| B、过氧化钠的结构式:Na-O-O-Na |
| C、K+离子的核外电子排布式:1s22s22p63s23p6 |
| D、丙烯酸(CH2=CHCOOH)分子中含9个σ键,1个π键 |