题目内容
下列离子方程式正确的是( )
| A、实验室中制取CO2:CO32-+2H+═CO2↑+H2O |
| B、钠投入CuSO4溶液中:2Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑ |
| C、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
| D、向酸性KMnO4溶液中滴加双氧水:2MnO4-+H2O2+6H+═2Mn2++3O2↑+4H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.实验室用碳酸钙与盐酸反应制取二氧化碳,碳酸钙为沉淀不能拆;
B.钠投入CuSO4溶液中,钠先与水反应生成氢氧化钠,然后氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀和硫酸钠;
C.向次氯酸钠溶液中通入足量SO2气体,反应生成硫酸和氯化钠;
D.氧化剂与还原剂得失电子数不守恒.
B.钠投入CuSO4溶液中,钠先与水反应生成氢氧化钠,然后氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀和硫酸钠;
C.向次氯酸钠溶液中通入足量SO2气体,反应生成硫酸和氯化钠;
D.氧化剂与还原剂得失电子数不守恒.
解答:
解:A.实验室中制取CO2离子方程式为:CaCO3+2H+═Ca2++CO2↑+H2O,故A错误;
B.钠投入CuSO4溶液中,离子方程式为:2Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑,故B正确;
C.向次氯酸钠溶液中通入足量SO2气体,离子方程式为:ClO-+SO2+H2O=SO42-+Cl-+2H+,故C错误;
D.向酸性KMnO4溶液中滴加双氧水,离子方程式为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故D错误;
故选:B.
B.钠投入CuSO4溶液中,离子方程式为:2Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑,故B正确;
C.向次氯酸钠溶液中通入足量SO2气体,离子方程式为:ClO-+SO2+H2O=SO42-+Cl-+2H+,故C错误;
D.向酸性KMnO4溶液中滴加双氧水,离子方程式为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故D错误;
故选:B.
点评:本题考查了离子方程式的书写,书写离子方程式关键在于明确化学反应的实质和离子方程式书写的方法,解题时注意化学式的拆分、反应是否符合客观事实.

练习册系列答案
相关题目
碳酸氢铵(NH4HCO3)是一种氮肥,其属于( )
| A、氧化物 | B、酸 | C、碱 | D、盐 |
“神舟六号”用动力燃料之一为氢化锂三兄弟--LiH、LiD、LiT.其中Li的质量数为7,有关下列叙述中正确的是( )
| A、三种物质质子数之比为1:2:3 |
| B、三种物质中子数之比为0:1:2 |
| C、三种物质的摩尔质量之比为4:5:6 |
| D、三种物质核外电子数之比为1:1:1 |
如果我们规定12C的相对原子质量为24,且0.024kg 12C中所含的原子个数为阿伏加德罗常数(NA),那么下列几种物理量(1)一个12C原子的质量;(2)阿伏加德罗常数(NA);(3)摩尔质量;(4)O2的相对分子质量;(5)气体摩尔体积;(6)agC2H5OH的物质的量;(7)98%浓硫酸的物质的量浓度;(8)44g CO2所含的分子个数.没有变化的是( )
| A、(1) |
| B、(1)(6)(7)(8) |
| C、(2)(3)(4)(5) |
| D、(1)(8) |
标准状况下,2mol Cl2和2mol H2O相比较,下列叙述中正确的是( )
| A、分子数相等 | B、原子数相等 |
| C、体积相等 | D、质量相等 |
如图所示实验合理的是( )
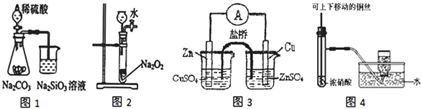

| A、图1证明非金属性强弱:S>C>Si |
| B、图2可制备少量氧气 |
| C、图3构成铜锌原电池,产生持续稳定的电流 |
| D、图4可制备并收集NO2气体 |
下列化学用语表示正确的是( )
A、CO(NH2)2的电子式: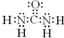 |
| B、NaHCO3的电离方程式:NaHCO3═Na++H++CO32- |
| C、1-丙醇的结构简式:C3H7OH |
| D、含18个中子的氯原子的核素符号:3517Cl |