题目内容
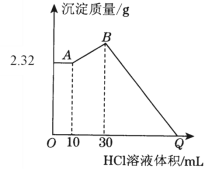
【题目】在25mL 0.1molL-1 NaOH溶液中逐滴加入0.2molL-1 CH3COOH溶液,曲线如图所示,下列判断正确的是( )

A. B点,a=12.5
B. D点,c(Na+)=c(CH3COO-)+c(CH3COOH)
C. 在C点升温,CH3COOH电离程度增大,CH3COO-的水解程度减小
D. 在A、B间存在一点,此点水的电离程度最大
【答案】D
【解析】
A.当a=12.5时,醋酸和氢氧化钠的物质的量相等,二者恰好反应生成醋酸钠,醋酸根离子部分水解,溶液显碱性,B点溶液呈中性,则加入的醋酸应该稍过量,即a>12.5,选项A错误;
B.D点,加入的醋酸的物质的量是氢氧化钠的物质的量的2倍,则2c(Na+)=c(CH3COO-)+c(CH3COOH),选项B错误;
C.升高温度,促进弱酸的电离和盐的水解,所以在C点升温,CH3COOH电离程度增大,CH3COO-的水解程度也增大,选项C错误;
D.酸碱抑制水的电离,能水解的盐促进水的电离,从A点开始,随着醋酸的加入,氢氧化钠的浓度减小,对水的电离的抑制程度减小,醋酸钠的浓度增大,对水的电离的促进制程度增大,当恰好生成醋酸钠时,对水的促进程度最大,继续加醋酸,水的电离程度又减小,即在A、B间存在一点,此点水的电离程度最大,选项D正确;
答案选D。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】依据下列实验现象,所得结论不正确的是
实验 | 实验现象 |
| ①品红溶液红色褪去,经检验溶液中含有SO42- ②加热褪色后的溶液至沸腾,未见颜色恢复,有气体溢出,可使蓝色石蕊试纸变红,遇淀粉碘化钾试纸,无明显变化。 |
A. 品红溶液褪色是氯水漂白所致
B. 集气瓶中发生了反应:Cl2 + SO2 + 2H2O H2SO4 + 2HCl
C. 依据现象②可确定产生的气体为SO2
D. 检验SO42-的试剂为:盐酸、BaCl2溶液