题目内容
【题目】用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。下列说法正确的是( )
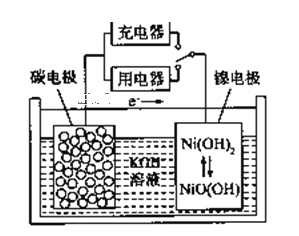
A. 充电时,阴极的电极反应为:Ni(OH)2+OH-+e-=NiO(OH)+H2O
B. 放电时,负极的电极反应为:H2-2e-+2OH-=2H2O
C. 放电时,OH-移向镍电极
D. 充电时,将电池的碳电极与外电源的正极相连
【答案】B
【解析】
开关连接用电器时,应为原电池原理,则根据电子流向,镍电极为正极得电子发生还原反应;开关连接充电器时,镍电极为阳极失电子发生的电极反应Ni(OH)2+OH--e-=NiO(OH)+H2O;
A.充电时,阴极上发生得电子的还原反应,即2H2O+2e-═H2↑+2OH-,故A错误;
B.放电时,负极上氢气失电子发生氧化反应,电极反应式为H2+2OH--2e-═2H2O,故B正确;
C.放电时,该电池为原电池,电解质溶液中阴离子向负极移动,所以OH-移向碳电极,故C错误;
D.该电池充电时,碳电极附近物质要恢复原状,则应该得电子发生还原反应,所以碳电极作阴极,应该与电源的负极相连,故D错误;
故答案为B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目