题目内容
(8分)为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。
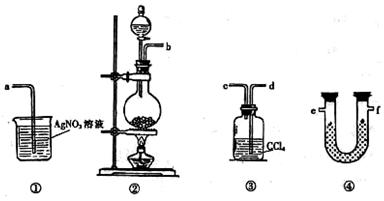
⑴请根据甲同学的意图,连接相应的装置,接口顺序:
b接________,__________接 _________,_________接a。
⑵U形管中所盛试剂的化学式为_____________________________ 。
⑶装置③中CCl4的作用是___________________________________。
⑷乙同学认为甲同学实验中有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在_____________之间(填装置序号)。瓶中可以放入______________________________________。
⑸丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成__________________________,如果观察到_______________________________________的现象,则证明制Cl2时有HCl挥发出来。


⑴请根据甲同学的意图,连接相应的装置,接口顺序:
b接________,__________接 _________,_________接a。
⑵U形管中所盛试剂的化学式为_____________________________ 。
⑶装置③中CCl4的作用是___________________________________。
⑷乙同学认为甲同学实验中有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在_____________之间(填装置序号)。瓶中可以放入______________________________________。
⑸丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成__________________________,如果观察到_______________________________________的现象,则证明制Cl2时有HCl挥发出来。
(8分) (1)e,f,d,c(2分) (2)CuSO4 (1分)
(3)吸收Cl2 (1分) (4)①③ (1分) 湿润的KI淀粉试纸(或湿润的有色布条)(1分)
(5)紫色石蕊试液(1分) 溶液变红且不褪色(1分)
(3)吸收Cl2 (1分) (4)①③ (1分) 湿润的KI淀粉试纸(或湿润的有色布条)(1分)
(5)紫色石蕊试液(1分) 溶液变红且不褪色(1分)
略

练习册系列答案
相关题目