题目内容
实验室有一瓶购置时间较长绿矾(FeSO4?7H2O),老师将其交给化学研究小组某同学检验药品是否有变质现象,这位同学取绿矾做了简单的检验,得出的结论是:已经开始氧化.该同学所用的试剂和判断依据是( )
| 选项 | A | B | C | D |
| 试剂 | 氯水 | 氢氧化钠溶液 | 铁屑 | KSCN溶液 |
| 现象 | 出现黄褐色 | 最终生成红褐色沉淀 | 绿色 | 有较浅的血红色 |
| A.A | B.B | C.C | D.D |
A.加入氯水,可将Fe2+氧化为Fe3+,不能检验是否变质,故A错误;
B.加入氢氧化钠溶液,生成的白色沉淀迅速变为灰绿色,最红变为红褐色,不能检验是否变质,故B错误;
C.加入铁屑,无论是否部分变质,最终都为浅绿色FeSO4溶液,不能检验是否变质,故C错误;
D.如变质,溶液中存在Fe3+,加入KSCN溶液,溶液变红,可检验,故D正确.
故选D.
B.加入氢氧化钠溶液,生成的白色沉淀迅速变为灰绿色,最红变为红褐色,不能检验是否变质,故B错误;
C.加入铁屑,无论是否部分变质,最终都为浅绿色FeSO4溶液,不能检验是否变质,故C错误;
D.如变质,溶液中存在Fe3+,加入KSCN溶液,溶液变红,可检验,故D正确.
故选D.

练习册系列答案
相关题目
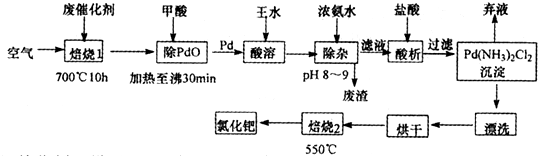
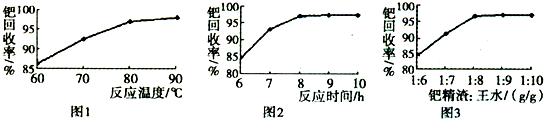
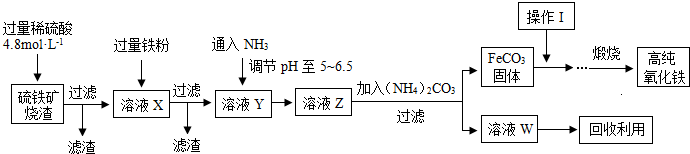
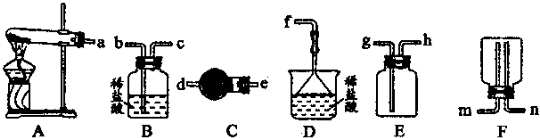
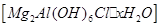 是一种新型离子交换材料,其在高温下完全分解为
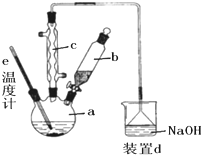
是一种新型离子交换材料,其在高温下完全分解为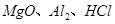 和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。
和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。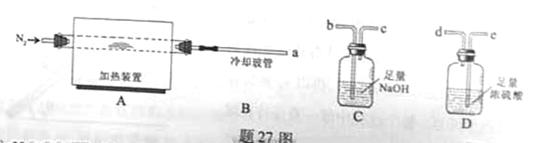
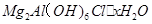 热分解的化学方程式为 。
热分解的化学方程式为 。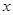 ,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。
,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。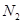 排尽装置中的空气,称取C、D的初始质量后,再持续通入
排尽装置中的空气,称取C、D的初始质量后,再持续通入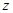 ,除测定D的增重外,至少还需测定 .
,除测定D的增重外,至少还需测定 .