题目内容
A、B、C、D、E是短周期的五种主族元素。A元素的某种原子,其核内没有中子;B元素的基态原子2p轨道上只有一对成对电子;C与B处于同一周期,且原子半径小于B;D与C是同主族元素;E元素的一价阳离子和C元素的阴离子具有相同的电子层结构。根据上述信息回答下列问题:
(1)B元素的原子结构示意图是 ;C元素原子的电子排布图是 ;D元素原子的价电子排布式是 ;
(2)A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是(用化学式表示) ;(3)由B、D、E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,写出该化合物的化学式 ;用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因 。
(1) (1分);
(1分);  ;3s23p5
;3s23p5
(2)HF>HCl (3)NaClO(1分);ClO-+H2O OH-+HClO (其它每项2分)
OH-+HClO (其它每项2分)
解析试题分析:A、B、C、D、E是短周期的五种主族元素。A元素的某种原子,其核内没有中子,则A是氢元素;B元素的基态原子2p轨道上只有一对成对电子,这说明2p轨道上有4个电子,则B元素氧元素;C与B处于同一周期,且原子半径小于B。根据同周期自左向右原子半径逐渐减小可知,C一定是氟元素;D与C是同主族元素,且属于短周期元素,因此D是氯元素;E元素的一价阳离子和C元素的阴离子具有相同的电子层结构,因此E是钠元素。
(1)氧元素位于周期表的第二周期第ⅥA族,所以其原子结构示意图是 ;F元素的原子序数是9,则根据构造原理、能量最低原理、洪特规则以及泡利原理可知,氟原子的电子排布图是
;F元素的原子序数是9,则根据构造原理、能量最低原理、洪特规则以及泡利原理可知,氟原子的电子排布图是 ;氯元素位于第三周期第ⅦA族,所以其原子的价电子排布式是3s23p5。
;氯元素位于第三周期第ⅦA族,所以其原子的价电子排布式是3s23p5。
(2)非金属性越强,氢化物的稳定性越强。同主族自上而下非金属性逐渐减弱,则非金属性强弱顺序是F>Cl 。因此A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是HF>HCl。
(3)由B、D、E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,这说明该化合物的水溶液显碱性,且还具有漂白性,因此该化合物是NaClO;次氯酸钠是强碱弱酸盐,溶于水ClO-水解溶液显碱性,水解方程式为ClO-+H2O OH-+HClO。因此用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因为ClO-+H2O
OH-+HClO。因此用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因为ClO-+H2O OH-+HClO。
OH-+HClO。
考点:考查元素周期表的结构、核外电子排布以及元素周期律的应用与判断

 阅读快车系列答案
阅读快车系列答案下表为部分短周期元素化合价及相应原子半径的数据:
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 原子半径(nm) | 0.102 | 0.110 | 0.117 | 0.074 | 0.075 | 0.071 | 0.099 | 0.077 |
| 最高化合价 | +6 | +5 | +4 | | +5 | | +7 | +4 |
| 最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
已知:
①A与D可形成化合物AD2、AD3;
②E与D可形成多种化合物,其中ED、ED2是常见的化合物,C可用于制光电池。
(1)E在周期表中位置是________________;
(2)C和H的气态氢化物的稳定性强弱关系为______________(用分子式表示);
(3)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是_____________________________________。
(4)工业上可用纯碱溶液处理ED和ED2,该反应如下:
ED+ED2+Na2CO3===2________+CO2
横线上某盐的化学式应为________。
(5)在一密闭容器中发生反应2AD2+D2
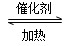 2AD3 ΔH=-47 kJ/mol,在上述平衡体系中加入18D2,当平衡发生移动后,AD2中18D的百分含量________(填“增加”“减少”或“不变”)其原因为______________________________________________
2AD3 ΔH=-47 kJ/mol,在上述平衡体系中加入18D2,当平衡发生移动后,AD2中18D的百分含量________(填“增加”“减少”或“不变”)其原因为______________________________________________(6)请设计一个实验方案,使铜和稀的H2AD4溶液反应,得到蓝色溶液和氢气。在下列方框内绘出该实验方案装置图。

J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等
| | | J | | |
| | | | | R |
M的气态原子逐个失去1~ 4个电子所需能量(电离能)如下表所示,
| | I1 | I2 | I3 | I4 | …… |
| 电离能(kJ/mol) | 578 | 1817 | 2745 | 11578 | …… |
(1)M的电子排布式为________;元素T在周期表中的位置为________。
(2)J和氢能形成多种化合物,其中分子成直线型的,且相对分子质量最小的物质的结构式为________。
(3)M和T形成的化合物在潮湿的空气中冒白雾,反应的化学方程式为_________________。
(4)由J、R形成的液态化合物JR2 0.2 mol在O2中完全燃烧,生成两种气态氧化物,298 K时放出热量215 kJ。该反应的热化学方程式为________。
(5)能源材料已成为当今科学研究的热点。氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。继C60后,科学家又合成了Si60、N60,下列有关说法正确的是_______(填序号)。
a. C60、Si60、N60都属于新型化合物
b. C60、Si60、N60互为同分异构体
c. 已知N60结构与C60相似,由于N-N键能小于N≡N,故N60的稳定性弱于N2
d. 已知金刚石中C-C键长154pm,C60中C-C键长145~140pm,故C60熔点高于金刚石
X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大。有关信息如下表:
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族。下列有关说法正确的是____________(填序号)。
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)X、Y组成的一种无色气体遇空气变为红棕色。将标准状况下40 L该无色气体与15 L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐。请写出该反应的离子方程式 。
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: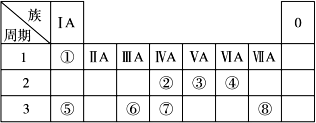
(1)地壳中含量居于第二位的元素在周期表中的位置是________________。
(2)②的最高价氧化物固态时的晶体类型:______________;⑦的最高价氧化物固态时的晶体类型:______________。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式______________,______________。若用球棍模型表示①和④形成的化合物的分子结构,应该是_____________。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是( )
| A.最高正化合价为+6价, | B.气态氢化物比H2S稳定, |
| C.最高价氧化物的水化物的酸性比硫酸弱, | D.单质在常温下可与氢气化合。 |
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
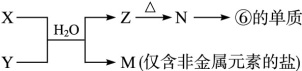
X溶液与Y溶液反应的离子方程式________, M中阳离子的鉴定方法____________。