题目内容
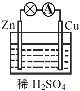
【题目】现有如下两个反应:(A)Cu2++Zn=Cu+Zn2+(B)2FeCl3+Cu=2FeCl2+CuCl2。
(1)分别画出两个实验装置图,注明电解质溶液名称和正负极材料,标出电子流动方向___、___。
(2)写出下列电极反应式:
①(A)中___是负极,负极反应式:___;
②(B)中___是负极,负极反应式:___。
【答案】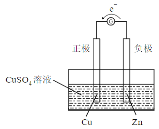
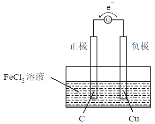 Zn Zn-2eˉ=Zn2+ Cu Cu-2eˉ=Cu2+
Zn Zn-2eˉ=Zn2+ Cu Cu-2eˉ=Cu2+
【解析】
(1)反应(A)Cu2++Zn=Cu+Zn2+中Cu2+被还原为正极反应,Zn被氧化为负极反应,所以原电池负极材料为Zn,电解质溶液可以选用可溶性铜盐如硫酸铜,正极材料可以选用Cu棒;原电池中电子由负极经外电路流向正极,装置图为: ;
;
反应(B)2FeCl3+Cu=2FeCl2+CuCl2中Fe3+被还原为正极反应,Cu被氧化为负极反应,所以原电池的负极材料为Cu,电解质溶液为FeCl3溶液,正极材料可以使C棒;原电池中电子由负极经外电路流向正极,装置图为: ;
;
(2)①(A)中Zn发生氧化反应为负极,电极反应式为Zn-2eˉ=Zn2+;
②(B)中Cu发生氧化反应为负极,电极反应式为Cu-2eˉ=Cu2+。

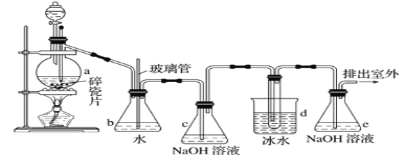
【题目】抗爆剂的添加剂常用1,2-二溴乙烷。如图为实验室制备1,2-二溴乙烷的装置图, 图中分液漏斗和烧瓶a中分别装有浓H2SO4和无水乙醇,d装罝试管中装有液溴。
相关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
密度/g·cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
熔点/℃ | -114.3 | 9.79 | - 116.2 | -7.2 |
水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装罝中导管是否发生堵塞,请写出发生堵塞时瓶b中的现象:①_____________________________;如果实验时d装罝中导管堵塞,你认为可能的原因是②___________________________________;
安全瓶b还可以起到的作用是③___________________________。
(2)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是_______________________。
(3)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正确情况下超过许多,如果装罝的气密性没有问题,试分析可能的原因:_____________________、_____________________________(写出两条即可)。
(4)除去产物中少量未反应的Br2后,还含有的主要杂质为________________,要进一步提纯,下列操作中必需的是
A.重结晶 B.过滤 C.萃取 D.蒸馏
(5)实验中也可以撤去d装置中盛冰水的烧杯,改为将冷水直接加入到d装置的试管中,则此时冷水除了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是___________。