题目内容
【题目】锑(Sb)广泛用于生产各种阻燃剂、陶瓷、半导体元件和医药及化工等领域。
Ⅰ.(1)锑在元素周期表中的位置_____。
(2)锑(Ⅲ)的氧化物被称为锑白,可以由SbCl3水解制得,已知SbCl3水解的最终产物为锑白。为了得到较多、较纯的锑白,操作时将SbCl3徐徐加入大量水中,反应后期还要加入少量氨水。试用必要的化学用语和平衡移动原理解释这两项操作的作用_______。工业上,还可用火法制取锑白,是将辉锑矿(主要成分为Sb2S3)装入氧化炉的坩埚中,高温使其融化后通入空气,充分反应后,经冷却生成锑白。写出火法制取锑白的化学方程式______。
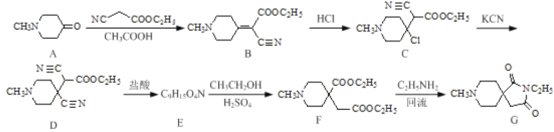
Ⅱ.以辉锑矿为原料制备金属锑,其中一种工艺流程如下:
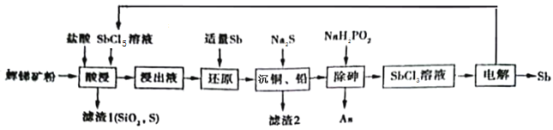
已知部分信息如下:
①辉锑矿(除Sb2S3外,还含有砷、铅、铜的化合物和SiO2等);
②浸出液主要含盐酸和SbCl3,还含SbCl5、CuCl2、AsCl3和PbCl2等杂质;
③常温下,Ksp(CuS)=1.0×10-36,Ksp(PbS)=9.0×10-29。
回答下列问题:
(3)“酸浸”过程中Sb2S3发生反应的化学方程式为_____。
(4)已知:浸出液中c(Cu2+)=0.0001mol/L,c( Pb2+)=0.1mol/L。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生沉淀的是_____(填化学式);当CuS、PbS共沉沉时,![]() =______(保留小数点后一位)。
=______(保留小数点后一位)。
(5)在“除砷”过程中,氧化产物为H3PO4。该反应氧化产物与还原产物的物质的量之比为__________。
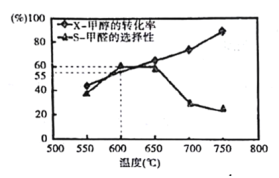
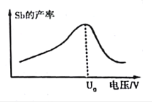
(6)在“电解”过程中,锑的产率与电压大小关系如图所示。当电压超过U0 V时,锑的产率降低的原因可能是_________。
【答案】第5周期第ⅤA族 2SbCl3+3H2O![]() Sb2O3+6HCl,不断加入SbCl3,使SbCl3浓度增大,利于水解平衡右移,反应后期加入氨水中和盐酸,使c(HCl)减小,利于平衡右移 2Sb2S3+9O2
Sb2O3+6HCl,不断加入SbCl3,使SbCl3浓度增大,利于水解平衡右移,反应后期加入氨水中和盐酸,使c(HCl)减小,利于平衡右移 2Sb2S3+9O2 ![]() 2Sb2O3+6SO2 Sb2S3+ 3SbCl5=5SbCl3+3S↓ CuS 1.1×10-8 3:4 H+参与电极反应
2Sb2O3+6SO2 Sb2S3+ 3SbCl5=5SbCl3+3S↓ CuS 1.1×10-8 3:4 H+参与电极反应
【解析】
Ⅱ.辉锑矿粉加入盐酸和SbCl5溶液,得到SbCl3和SbCl5溶液,还含有杂质CuCl2、AsCl3和PbCl2等,加入适量Sb将SbCl5还原为SbCl3,加入Na2S使铜和铅沉淀以除去CuCl2和PbCl2,然后加入NaHPO2除去杂质砷。得到的SbCl3溶液电解得到金属Sb,同时得到SbCl5,可以返回到酸浸步骤循环使用。
Ⅰ.(1)锑和氮在同一主族,其在元素周期表中位于第5周期第ⅤA族。
(2)SbCl3水解:2SbCl3+3H2O![]() Sb2O3+6HCl,将SbCl3徐徐加入大量水中,SbCl3浓度增大,水解平衡右移,反应后期还要加入少量氨水中和HCl,使c(HCl)减小,平衡右移,有利于Sb2O3的生成。故答案为:2SbCl3+3H2O
Sb2O3+6HCl,将SbCl3徐徐加入大量水中,SbCl3浓度增大,水解平衡右移,反应后期还要加入少量氨水中和HCl,使c(HCl)减小,平衡右移,有利于Sb2O3的生成。故答案为:2SbCl3+3H2O![]() Sb2O3+6HCl,不断加入SbCl3,使SbCl3浓度增大,利于水解平衡右移,反应后期加入氨水中和盐酸,使c(HCl)减小,利于平衡右移。
Sb2O3+6HCl,不断加入SbCl3,使SbCl3浓度增大,利于水解平衡右移,反应后期加入氨水中和盐酸,使c(HCl)减小,利于平衡右移。
火法制取锑白,是辉锑矿(主要成分为Sb2S3)在高温下和空气中的氧气反应,生成Sb2O3的同时生成SO2。化学方程式为:2Sb2S3+9O2 ![]() 2Sb2O3+6SO2。
2Sb2O3+6SO2。
Ⅱ.(3)“酸浸”时Sb2S3和SbCl5溶液反应,得到SbCl3和SbCl5的混合溶液,滤渣中有硫,是此反应的生成物,Sb2S3发生反应的化学方程式为Sb2S3+ 3SbCl5=5SbCl3+3S。
(4)浸出液中c(Cu2+)=0.0001mol/L,c(Pb2+)=0.1mol/L。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,当Cu2+开始沉淀时,c(S2-)=![]() =1.0×10-32mol/L,当Pb2+开始沉淀时,c(S2-)=
=1.0×10-32mol/L,当Pb2+开始沉淀时,c(S2-)=![]() =9.0×10-28mol/L,所以先产生沉淀的是CuS;当CuS、PbS共沉淀时,
=9.0×10-28mol/L,所以先产生沉淀的是CuS;当CuS、PbS共沉淀时,![]() =
=![]() =
=![]() =
=![]() =1.1×10-8。
=1.1×10-8。
(5)加入NaHPO2除砷,发生了NaHPO2和AsCl3的反应,氧化产物为H3PO4,还原产物是As,磷的化合价从/span>+1价升高到+5价,生成1mol H3PO4失去4mol电子,砷的化合价从+3价降低到0价,生成1molAs得到3mol电子,根据电子守恒,该反应氧化产物与还原产物的物质的量之比为3:4。
(6)电解SbCl3溶液制取锑,在阴极是Sb3+得到电子生成Sb,当电压过大时,溶液中的H+也可能在阴极放电,导致锑的产率降低。

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案【题目】碳酸镁晶须是一种新型的吸波隐形材料中的增强材料。
(1)合成该物质的步骤如下:
步骤1:配制0.5mol·L-1 MgSO4溶液和0.5mol·L-1 NH4HCO3溶液。
步骤2:用量筒量取500mL NH4HCO3溶液于1000mL三颈烧瓶中,开启搅拌器。温度控制在50℃。
步骤3:将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min内滴加完后,用氨水调节溶液pH到9.5。
步骤4:放置1h后,过滤,洗涤。
步骤5:在40℃的真空干燥箱中干燥10h,得碳酸镁晶须产品(MgCO3·nH2O n=1~5)。
①步骤2控制温度在50℃,较好的加热方法是_________。
②步骤3生成MgCO3·nH2O沉淀的化学方程式为__________。
③步骤4检验沉淀是否洗涤干净的方法是__________。
(2)测定生成的MgCO3·nH2O中的n值。
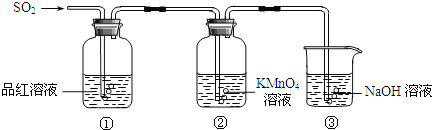
称量1.000碳酸镁晶须,放入如图所示的广口瓶中加入适量水,并滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5h,反应后期将温度升到30℃,最后将烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次。
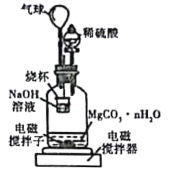
①图中气球的作用是_________。
②上述反应后期要升温到30℃,主要目的是______。
③测得每7.8000g碳酸镁晶须产生标准状况下CO2为1.12L,则n值为_______。
(3)碳酸镁晶须可由菱镁矿获得,为测定某菱镁矿(主要成分是碳酸镁,含少量碳酸亚铁、二氧化硅)中铁的含量,在实验室分别称取12.5g菱镁矿样品溶于过量的稀硫酸并完全转移到锥形瓶中,加入指示剂,用0.010mol/L H2O2溶液进行滴定。平行测定四组。消耗H2O2溶液的体积数据如表所示。
实验编号 | 1 | 2 | 3 | 4 |
消耗H2O2溶液体积/mL | 15.00 | 15.02 | 15.62 | 14.98 |
①H2O2溶液应装在_________(填“酸式”或“碱式”)滴定管中。
②根据表中数据,可计算出菱镁矿中铁元素的质量分数为_________ %(保留小数点后两位)。