题目内容
【题目】运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
I.氨为重要的化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a. CH4(g)+H2O(g)CO(g)+3H2(g) H1=+216.4kJ/mol
b. CO(g)+H2O(g)CO2(g)+H2(g) H2=-41.2kJ/mol
则反应CH4(g)+2H2O(g)CO2(g)+4H2(g) H= _____________。
(2)起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。
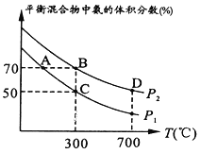
①恒压时,反应一定达到平衡状态的标志是_____________(填序号)
A.![]() 和
和![]() 的转化率相等 B.反应体系密度保持不变
的转化率相等 B.反应体系密度保持不变
C.![]() 保持不变 D.
保持不变 D.![]()
②P1_____P2 (填“<”或“>”或“=”或“不确定”,下同);反应的平衡常数:B点_______D点。
③C点![]() 的转化率为________;在A、B两点条件下,该反应从开始到平衡时生成氮气的平均速率:υ(A)__________υ(B)。
的转化率为________;在A、B两点条件下,该反应从开始到平衡时生成氮气的平均速率:υ(A)__________υ(B)。
【答案】+175.2kJ/mol BC < > 66.7% <
【解析】
(1)已知:a. CH4(g)+H2O(g)CO(g)+3H2(g) H1=+216.4kJ/mol
b. CO(g)+H2O(g)CO2(g)+H2(g) H2=-41.2kJ/mol
则将a+b可得CH4(g)+2H2O(g)CO2(g)+4H2(g) H= (+216.441.2)kJ/mol=+175.2kJ/mol
答案为:+175.2kJ/mol
(2)①A.N2和H2的物料比为1:3,且按照1:3反应,则无论是否达到平衡状态,转化率都相等,不能用于判断是否达到平衡状态,故A错误;
B. 气体的总质量不变,恒压条件下,当反应体系密度保持不变时,说明体积不变,则达到平衡状态,故B正确;
C.![]() 比值为保持不变,说明氮气、氨气的浓度不变,能确定是否达到平衡状态,故C正确;
比值为保持不变,说明氮气、氨气的浓度不变,能确定是否达到平衡状态,故C正确;
D. 因平衡常数等未知,![]() ,不能确定是否平衡状态,故D错误。
,不能确定是否平衡状态,故D错误。
故答案为:BC;
②增大压强,平衡正向移动,平衡混合气体中氨气的百分含量增大,由图象可知P1<P2,升高温度,平衡逆向移动,平衡常数减小,则反应平衡常数:B点>D点,
故答案为:<;>;
③起始时投入氮气和氢气分别为1mol、3mol,反应的方程式为N2(g)+3H2(g)2NH3(g),C点氨气的含量为50%,则
N2(g)+3H2(g)2NH3(g)
起始:1mol3mol0
转化:xmol3xmol2xmol
平衡:(1x)mol(33x)mol2xmol
则![]() =50%,x=
=50%,x=![]() ,
,
C点H2的转化率为![]() ×100%=66.7%,温度越高,反应速率越大,则v(A)<v(B),
×100%=66.7%,温度越高,反应速率越大,则v(A)<v(B),
故答案为:66.7%;<;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案