题目内容
【题目】(1)化合物A是一种不稳定的物质,它的分子组成可用OxFy表示。10mLA气体 能分解生成15mLO2和10mLF2(在同温同压下),A的化学式是_____。
(2)VLFe2(SO4)3溶液中含有agSO42-,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中 Fe3+的物质的量的浓度为____。
【答案】O3F2 a/576mol/L
【解析】
(1)相同条件下,气体的体积之比等于其物质的量之比,同一反应中,参加反应的各物质的物质的量之比等于其计量数之比,再结合质量守恒确定A化学式.
(2)根据n=![]() 计算出硫酸根离子的物质的量,从而可计算出0.5L溶液中含有的硫酸根离子,然后根据稀释过程中溶质的物质的量不变计算出稀释后溶液中铁离子的物质的量,最后根据c=
计算出硫酸根离子的物质的量,从而可计算出0.5L溶液中含有的硫酸根离子,然后根据稀释过程中溶质的物质的量不变计算出稀释后溶液中铁离子的物质的量,最后根据c=![]() 计算出稀释后溶液中Fe3+的物质的量的浓度.
计算出稀释后溶液中Fe3+的物质的量的浓度.
(1)相同条件下,气体的体积之比等于其物质的量之比,同一反应中,参加反应的各物质的物质的量之比等于其计量数之比,所以参加反应的A、O2、F2的计量数之比=10mL:15mL:10mL=2:3:2,再结合质量守恒定律得A中含有3个O、2个F原子,O电负性小于F元素,所以二者形成的化合物A中O显正化合价、F元素显负化合价,所以A的化学式为O3F2,
故答案为:O3F2;
(2)ag硫酸根离子的物质的量为:![]() ,取出的0.5VL溶液中含有硫酸根离子的物质的量为:
,取出的0.5VL溶液中含有硫酸根离子的物质的量为:![]() mol×0.5V÷VL=a/192mol,
mol×0.5V÷VL=a/192mol,
稀释过程中溶质的物质的量不变,则稀释后溶液中铁离子物质的量为:a/192mol×2/3=a/288mol,
则稀释后溶液中铁离子浓度为:a/288mol÷2VL=a/576mol/L,
故答案为:a/576mol/L。

【题目】氢气是一种重要的清洁能源。
(1)航天员呼吸产生的![]() 利用
利用![]() 反应:
反应:![]() H,再电解水可实现
H,再电解水可实现![]() 的循环利用。
的循环利用。
①热力学中规定,由最稳定单质生成![]() 某物质的焓变称为该物质的标准生成焓(符号:
某物质的焓变称为该物质的标准生成焓(符号:![]() ),最稳定单质的标准生成焓规定为0。已知上述反应式中:
),最稳定单质的标准生成焓规定为0。已知上述反应式中:
![]() ;
;![]() ;
;![]() ;
;
![]() ;则
;则![]() _____
_____![]() 。
。
②![]() 反应必须在高温下才能进行,原因是___________________________。
反应必须在高温下才能进行,原因是___________________________。
③350℃时,向体积为![]() 的恒容密闭容器中通入
的恒容密闭容器中通入![]() 和
和![]() 发生以上反应。
发生以上反应。
测得反应过程中压强随时间的变化如下表所示:
时间/ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
压强 |
|
|
|
|
|
|
|
350℃时![]() 反应的
反应的![]() ______(
______(![]() 为用气体的分压代替各组分平衡浓度表示的平衡常数,气体分压=气体的体积分数×体系总压)。
为用气体的分压代替各组分平衡浓度表示的平衡常数,气体分压=气体的体积分数×体系总压)。
(2)利用乙醇重整制氢是获得氢能的研究热点,其主要反应原理为:
反应Ⅰ: ![]() H1
H1
若同时通入水蒸汽,还会发生如下反应
反应Ⅱ:![]() H2
H2
反应Ⅲ:![]() H3
H3
反应Ⅳ:![]() H4
H4
一定温度下,某恒压密闭容器中充入一定量的![]() 发生反应。
发生反应。
已知:氢气选择性指转化的原料气中,转化成氢气的氢元素质量与转化的氢元素总质量的比值。
①下列有关说法正确的是_______________。
A.当混合气的平均相对分子质量不变时,说明反应达到平衡状态
B.增大乙醇初始浓度,能够提高乙醇的平衡转化率
C.其它条件不变,掺入稀有气体,可提高乙醇平衡转化率
D.其它条件不变,掺入水蒸气,可提高氢气的选择性和氢气的体积分数
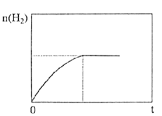
②下图为上述条件下n(H2)随反应时间的变化曲线图。若其它初始条件相同,只把容器变为恒容密闭容器,请画出恒容条件下,n(H2)随反应时间的变化曲线图________________。
③乙醇重整制氢过程中,还可能生成固态炭,固态炭的生成会造成催化剂失活,应尽量避免。研究其它条件相同下,反应温度、氧醇比、水醇比与生成固态炭的条件,得到下图:
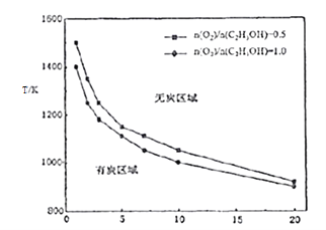
试根据图象分析,反应温度、氧醇比、水醇比对固态炭生成的影响_____________。