��Ŀ����
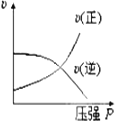
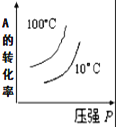
����Ŀ����1L�ܱ������н������·�Ӧ��X��g��+3Y��g��![]() 2Z��g�����ﵽƽ��ʱ X��Y��Z�����ʵ����ֱ�Ϊ 0.1mol��0.3mol��0.2mol�������¶Ⱥ������������ʱ�����������г���X��Y��Z�����ʵ���0.1mol��0.3mol��0.2mol��������˵����ȷ����
2Z��g�����ﵽƽ��ʱ X��Y��Z�����ʵ����ֱ�Ϊ 0.1mol��0.3mol��0.2mol�������¶Ⱥ������������ʱ�����������г���X��Y��Z�����ʵ���0.1mol��0.3mol��0.2mol��������˵����ȷ����
A. ��ѧƽ�ⳣ�����䣬ƽ�ⲻ�ƶ� B. ������Ӧ�����ƶ�
C. ���淴Ӧ�����ƶ� D. ������ѹǿʼ�ձ���ԭ����2��
���𰸡�B
��������
��������ݿ�֪�����μ���������ͬ�ģ���Ϊ���µ�ѹ���������ܽ�����Чƽ�⣬�������ǵ��µ��ݣ����൱������ѹǿ��ƽ���Ӱ�죬��������Ӧ�����������С�ķ�Ӧ����������ѹǿƽ��������Ӧ�����ƶ����Դ˷������
A. ƽ�ⳣ��ֻ���¶��йأ��¶Ȳ��䣬ƽ�ⳣ�����䣬��ƽ���������ƶ�����A����
B. ���µ��������������������г���X��Y��Z�����ʵ���0.1mol��0.3mol��0.2mol�����൱�ڼ�ѹ��ƽ��������Ӧ�����ƶ�����B��ȷ��
C. �������Ϸ�����ƽ��������Ӧ�����ƶ�����C����
D. ƽ��������Ӧ�����ƶ����������ʵ�����С��ѹǿҲ�����ı䣬��D����
�ʴ�ѡB��

��ϰ��ϵ�д�
 ͬ��������ϰϵ�д�
ͬ��������ϰϵ�д� �ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
�ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
�����Ŀ