题目内容
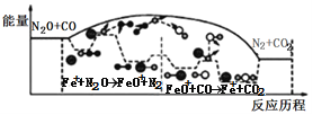
【题目】研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是
A.反应总过程是放热的
B.Fe+作为催化剂改变了反应途径,提高了反应速率
C.Fe++N2O→FeO++N2、FeO++CO→Fe++CO2 两步反应均为放热反应
D.若反应在恒容密闭容器中进行,温度越高,反应速率一定越快
【答案】D
【解析】
由图可知,N2O与CO的反应是放热反应,它们在Fe+做催化剂作用下发生Fe++N2O→FeO++N2、FeO++CO→Fe++CO2反应,都是总能量降低,都是放热反应。
A.由图可知,N2O与CO反应前后总能量降低,是放热反应,A正确;
B.由Fe++N2O→FeO++N2、FeO++CO→Fe++CO2可知,Fe+先消耗后生成,总量保持不变,起催化剂作用,B正确;
C.由图可知,Fe++N2O→FeO++N2、FeO++CO→Fe++CO2反应,都是总能量降低,都是放热反应,C正确;
D.该反应使用了Fe+做催化剂,催化剂的活性与温度有关,只有在适当的温度范围内才能发挥催化剂的催化活性,所以温度越高,反应速率不一定越快,D错误;
答案选D。

练习册系列答案
相关题目