题目内容
8.VL Al2(SO4)3溶液中含有mg Al3+,则溶液中Al2(SO4)3的物质的量浓度是$\frac{m}{54V}$mol/L.分析 根据n=$\frac{m}{M}$计算Al3+的物质的量,溶液中n[Al2(SO4)3]=$\frac{1}{2}$n(Al3+),再根据c=$\frac{n}{V}$计算Al2(SO4)3溶液的物质的量浓度.
解答 解:mgAl3+的物质的量=$\frac{mg}{27g/mol}$=$\frac{m}{27}$mol,
溶液中n[Al2(SO4)3]=$\frac{1}{2}$n(Al3+)=$\frac{1}{2}$×$\frac{m}{27}$mol=$\frac{m}{54}$mol,
故c[Al2(SO4)3]=$\frac{\frac{m}{54}mol}{VL}$=$\frac{m}{54V}$mol/L,
故答案为:$\frac{m}{54V}$mol/L.
点评 本题考查物质的量浓度的有关计算,难度不大,注意理解电解质与电解质离子物质的量之间的关系.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
18.钢铁发生吸氧腐蚀时,发生还原反应的电极反应式是( )
| A. | Fe→Fe2++2e- | B. | 2H++2e-→H2↑ | ||
| C. | 4OH-→2H2O+O2↑+4e- | D. | 2H2O+O2+4e-→4OH- |
19.下列几种物质中不属于天然高分子化合物的是( )
| A. | 聚乙烯 | B. | 淀粉 | C. | 纤维素 | D. | 蛋白质 |
16.在pH=1的溶液中,因发生氧化还原反应而不能大量共存的离子组是( )
| A. | Ca2+、Cl-、HCO3-、K+ | B. | ClO-、K+、SO42-、Ba2+ | ||
| C. | CH3COO-、K+、Na+、CO32- | D. | Fe2+、Ag+、NO3-、K+ |
3.下列事实,不能用勒夏特列原理解释的是( )
| A. | 反应CO+NO2?CO2+NO△H<0,升高温度可使平衡向逆反应方向移动 | |
| B. | 合成NH3的反应,为提高NH3的产率,理论上应采取相对较低温度的措施 | |
| C. | 溴水中存在平衡:Br2+H2O?HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 | |
| D. | 对2HI(g)?H2(g)+I2(g),增大平衡体系的压强(压缩体积)可使体系颜色变深 |
20.在密闭容器中,下列可逆反应达到平衡后,升高温度可以使混合气体平均相对分子质量减小的是( )
| A. | H2(气)+Br2(气)?2HBr(气)△H<0 | B. | N2(气)+3H2(气)?2NH3(气)△H<0 | ||
| C. | N2O4?2NO2 △H>0 | D. | 4NH3(气)+5O2(气)?4NO(气)+6H2O(气)△H<0 |
17.下列化学方程式的配平正确的是( )
| A. | 2KMnO4+11H2S+5H2SO4→K2SO4+2MnSO4+13S↓+16H2O | |
| B. | 2KMnO4+8H2S+4H2SO4→K2SO4+2MnSO4+9S↓+12H2O | |
| C. | 2KMnO4+5H2S+3H2SO4→K2SO4+2MnSO4+S↓+4H2O | |
| D. | 2KMnO4+5H2S+3H2SO4→K2SO4+2MnSO4+5S↓+8H2O |
12.下列有关食品添加剂的说法正确的是( )
| A. | 需要长时间储存的食品应加入适宜的防腐剂 | |
| B. | 冰激凌不使用着色剂营养价值一定会降低 | |
| C. | 色、香、味俱全的食物营养价值不一定高 | |
| D. | 炒菜时拒绝添加食盐、味精等各种调味剂 |
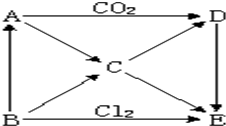 下图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为金属单质.试推出各物质的化学式,并写出有关反应的化学方程式.
下图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为金属单质.试推出各物质的化学式,并写出有关反应的化学方程式.