题目内容
【题目】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+ O2 (g)![]() 2SO3(g) ΔH<0
2SO3(g) ΔH<0
(1)降低温度,该反应K值______,二氧化硫转化率____,化学反应速度____ ,(以上均填增大、减小或不变)
(2)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是_____。
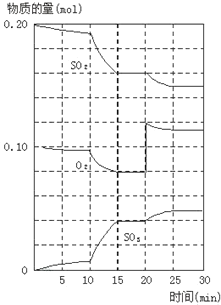
(3)据图判断,反应进行至20min时,曲线发生变化的原因_____(用文字表达)
(4)10min到15min的曲线变化的原因可能是____(填写编号)。
a.加了催化剂 b.缩小容器体积 c.降低温度 d.增加SO3的物质的量
【答案】增大 增大 减小 15-20min、25-30min 增大氧气的浓度 ab
【解析】
(1)降温,放热反应平衡正移,K增大,反应物转化率增大,速率减小;
(2)各组分的物质的量不变,反应处于平衡状态;
(3)找断点,瞬间只有氧气的浓度增大,应是增大了氧气的浓度;
(4)10min到15min的曲线斜率变大,反应方向不变,且没有出现断点。
(1)该反应正反应为放热反应,降低温度平衡向正反应方向移动,平衡常数K增大,二氧化硫转化率增大,降低温度反应速率减小;
(2)反应混合物各物质的物质的量不变化,说明反应处于平衡状态,由图可知在15-20min和25-30min出现平台,各组分的物质的量不变,反应处于平衡状态;
(3)由图可知,反应进行至20min时,平衡向正反应移动,瞬间只有氧气的浓度增大,应是增大了氧气的浓度;
(4)由图可知,反应向正反应进行,10min到15min反应混合物单位时间内的变化量增大,说明反应速率增大;且10min改变瞬间,各物质的物质的量不变。
a.加了催化剂,增大反应速率,故a正确;
b.缩小容器体积,增大压强,增大反应速率,故b正确;
c.降低温度反应速率降低,故c错误;
d.10min改变瞬间,各物质的物质的量不变,不是增加SO3的物质的量,故d错误;
答案选ab。

 启东小题作业本系列答案
启东小题作业本系列答案