题目内容
7.石墨是层状晶体,每一层内碳原子排列成正六边形,一个个六边形排列成平面的网状结构.如果将每对相邻原子间的化学键看成是一个化学键,则石墨晶体每一层内碳原子数与碳-碳化学键数的比是( )| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 2:3 |
分析 每一层内碳原子排列成正六边形,每个C原子连接3个C-C键,则每个C原子平均含有C-C个数=$\frac{1}{2}$×3,据此分析解答.
解答 解:每一层内碳原子排列成正六边形,每个C原子连接3个C-C键,则每个C原子平均含有C-C个数=$\frac{1}{2}$×3=1.5,则石墨晶体每一层内碳原子数与碳-碳化学键数的比=1:1.5=2:3,故选D.
点评 本题考查石墨中原子与化学键的有关计算,侧重考查学生分析计算能力,采用均摊法分析解答即可,题目难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
17.常温下pH=9的Ca(OH)2溶液与pH=13的NaOH溶液按体积比4:1混合,溶液中氢离子的浓度(mol/L)为( )
| A. | 5.0×10-13 | B. | 2.0×10-12 | ||
| C. | $\frac{1}{5}$(1×10-+4×10-5) | D. | $\frac{1}{5}$(1×10-13+4×10-9) |
18.下列叙述正确的为( )
| A. | 石墨转化为金刚石属于化学变化 | |
| B. | 金刚石和石墨具有相似的物理性质 | |
| C. | C60是碳元素的一种单质,其摩尔质量为720 | |
| D. | 由碳元素单质组成的物质一定是纯净物 |
19.下列离子方程式正确的是( )
| A. | Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 将Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| C. | MnO2与浓盐酸共热制Cl2:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| D. | Cl2通入冷的NaOH溶液中:2Cl2+2OH-═3Cl-+ClO-+H2O |
17.醋酸的电离方程式为CH3COOH(aq)?H+(aq)+CH3COO-(aq)△H>0.25℃时,0.1mol/L醋酸溶液中存在下述关系:$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=1.75×10-5,其中的数值是该温度下醋酸的电离平衡常数(Ka).下列说法正确的是( )
| A. | 向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小 | |
| B. | 向该溶液中加入少量CH3COONa固体,平衡正向移动 | |
| C. | 该温度下0.01mol/L醋酸溶液Ka<1.75×10-5 | |
| D. | 升高温度,c(H+)增大,Ka变大 |

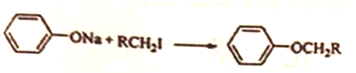

 .
.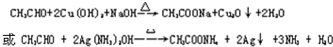 .
.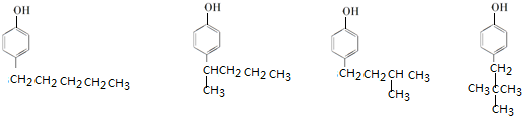 、
、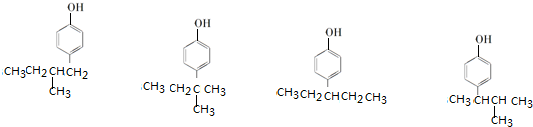 (其中任意两种).
(其中任意两种).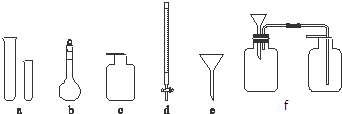
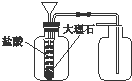 .
.