题目内容
【题目】下列能使品红溶液褪色的是( )
A. SO2 B. BaSO4 C. KCl D. CO2
【答案】A
【解析】SO2与品红发生化合反应生成无色物质,可使品红褪色,而BaSO4、KCl、CO2不能使品红溶液褪色,故选A。
具有漂白性的物质 | |||
物质 | HClO、O3、H2O2、Na2O2 | SO2 | 木炭 |
原理 | 将有色物质氧化分解 | 与有色物质结合生成无色物质 | 将有色物质的分子吸附在其表面 |
实质 | 氧化还原反应 | 非氧化还原反应 | 物理吸附 |
效果 | 永久性 | 暂时性 | 暂时性 |
范围 | 可漂白大多数有色物质,能使紫色石蕊褪色 | 可漂白某些有色物质,不能使石蕊试液褪色 | 可吸附某些有色物质的分子 |

【题目】中和热的测定是重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于下图所示的装置中进行中和热的测定实验,回答下列问题:
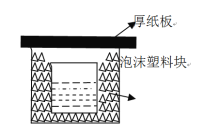
(1)从图中实验装置看,其中尚缺少的两种玻璃用品是_,为保证该实验成功,该同学采取了许多措施,如图的泡沫塑料块的作用在于。
(2)倒入NaOH溶液的正确操作是:(从下列选出)。
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
D.简述测量温度的方法
(3)实验记录数据如表
项目 | 反应起始温度T1(℃) | 终止温度T2(℃) | T2-T1 | ||
HCl | NaOH | 平均温度 | |||
第1次 | 26.2 | 26.0 | 29.4 | ||
第2次 | 27.0 | 27.4 | 32.2 | ||
第3次 | 25.9 | 25.9 | 29.1 | ||
第4次 | 26.4 | 26.2 | 29.7 | ||
设0.55mol/LNaOH溶液和0.50mol/L盐酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=(取到小数点后一位)。
(4)不能用醋酸代替盐酸做此实验,原因是____________________。
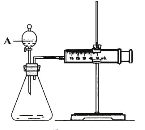
【题目】用如下图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0.7克镁带,按右图连接好装置,从A中加入20.0ml0.5mol/LH2SO4。记录注射器活塞的位置和相应的时间。记录数据如下
时间/s | 0 | t | 2t | ...... |
活塞的位置/ml | 17.3 | 25.6 | 36.6 | ...... |
(1)检查该装置气密性的方法是。
(2)仪器A的名称是。
(3)0-t时间段与t-2t时间段,化学反应速率最快的是,原因是。
(4)用上述装置探究Fe3+、Cu2+对双氧水分解速率的影响,所用试剂:5%H2O2、0.1mol/LFeCl3、0.2mol/LCuCl2,完成下表的实验设计:
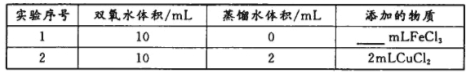
①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:___________。
②上表中需要添加的物质是mlFeCl3溶液。
③本实验需要测定的数据是。
(5)为确定MnO2催化双氧水分解的最佳条件,用该实验装置进行实验,反应物用量和反应停止的时间数据如下表。
MnO2 时间 H2O2 | 0.1g | 0.3g | 0.8g |
10mL1.5% | 223s | 67s | 36s |
10mL3.0% | 308s | 109s | 98s |
10mL4.5% | 395s | 149s | 116s |
分析表中数据回答下列问题:
①相同浓度的过氧化氢的分解速率随着MnO2用量的增加而_______(填“加快”、“减慢”或“不变”)。
②从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入__________g的MnO2为较佳选择。
③该小组的某同学分析上述数据后认为:“当用相同质量的MnO2时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确?______(填“正确”或“不正确”),理由是_________________________。(提示:H2O2溶液的密度可认为近似相等。)