题目内容
【题目】Ⅰ.肼(N2H4)又称联氨,常温时是一种可燃性液体,可用作火箭燃料。
(1)已知在25℃、101kPa时,16g N2H4在氧气中完全燃烧生成氮气,放出312kJ的热量,则N2H4完全燃烧的热化学方程式是_______________。
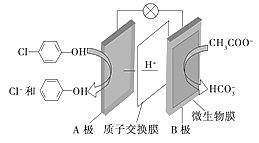
Ⅱ.如图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)—空气燃料电池(如图甲)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。
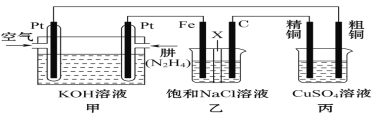
根据要求回答相关问题:
(2)甲装置中通入_________气体的一极为正极,负极的电极反应式为__________。
(3)乙装置中石墨电极为______极,其电极反应式为___________;可以用______________检验该反应产物,电解一段时间后,乙池中的溶液呈__________性。
(4)图中用丙装置模拟工业中的_____________________原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为____________g。
(5)如果将丙中的粗铜电极换为Pt电极,则丙中总化学方程式为_______________。
【答案】N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624kJ/mol 空气 N2H4-4e-+4OH-=4H2O+N2↑ 阳 2Cl--2e-=Cl2↑ 湿润的淀粉碘化钾试纸 碱 粗铜的精炼 0.8 2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4
2Cu+O2↑+2H2SO4
【解析】
依据热化学方程式书写方法,标注物质聚集状态和对应量的反应热写出热化学方程式;乙装置中石墨电极与电源正极连接,为阳极,阳极上是氯离子放电生成氯气,检验氯气的方法是用湿润的淀粉碘化钾试纸,观察是否变蓝,根据电解总反应方程式,判断溶液的酸碱性;根据同一闭合回路中转移电子相等,列出关系式:N2H4~2Cu进行分析求解;Pt电极为惰性电极,用惰性电极电解CuSO4溶液,根据离子放电的先后顺序确定溶液的总反应方程式。
(1)16.0g气态肼(N2H4)物质的量为n(N2H4)=16g÷32g/mol=0.5mol,在氧气中完全燃烧生成氮气和水,放出热量312kJ,1mol气态肼(N2H4)燃烧放热624kJ,反应的热化学方程式为:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624kJ/mol;
(2)甲装置中通入空气的电极为正极,正极上空气中的氧气得电子发生还原反应,电极反应式为:O2+4e-+2H2O=4OH-,负极N2H4失去电子发生氧化反应,电极反应式为:N2H4-4e-+4OH-=4H2O+N2↑;
(3)根据装置图可知:乙装置中石墨电极连接甲装置的正极,作阳极,在阳极上是氯离子放电生成氯气,电极反应式为:2Cl--2e-=Cl2↑;检验氯气的方法是用湿润的淀粉碘化钾试纸,若观察到湿润的淀粉碘化钾试纸变蓝,就证明有氯气产生;阳极为惰性电极,电解饱和食盐水的总反应方程式为:2NaCl+2H2O![]() Cl2↑+H2↑+2NaOH,可见电解一段时间后,乙池中的溶液呈碱性;
Cl2↑+H2↑+2NaOH,可见电解一段时间后,乙池中的溶液呈碱性;
(4)丙装置中粗铜连接电源的正极,作阳极,精铜连接电源的负极,作阴极,电解质为硫酸铜溶液,因此图中用丙装置模拟工业中的铜的精炼原理;由于在同一闭合回路中电子转移数目相等,所以根据关系式:N2H4~2Cu,n(Cu)=3.2g÷64g/mol=0.05mol,所以n(N2H4)=![]() n(Cu)=
n(Cu)=![]() ×0.05mol=0.025mol,则m(N2H4)=0.025mol×32g/mol=0.8g;
×0.05mol=0.025mol,则m(N2H4)=0.025mol×32g/mol=0.8g;
(5)如果将丙中的粗铜电极换为Pt电极,由于Pt电极为惰性电极,因此阳极上是溶液中的OH-失去电子,变为O2,阴极上,溶液中的Cu2+获得电子变为Cu单质,所以丙中总化学方程式为2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4。
2Cu+O2↑+2H2SO4。

【题目】钛是一种活泼金属。从高钛渣(主要为TiO2)提炼海绵钛流程如下:
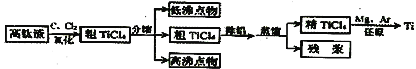
氯化后的粗TiCl4中含有FeCl3、SiCl4、AlCl3等杂质,相关物质的沸点如下表:
化合物 | TiCl4 | FeCl3 | SiCl4 | AlCl3 |
沸点/℃ | 136 | 310 | 56.5 | 180 |
下列说法不正确的是( )
A.“氯化”反应的尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是H2O、FeCl2溶液、NaOH溶液
B.“分馏”得到的低沸点物为SiCl4,高沸点物为FeCl3
C.己知“除铝”的方法是用水湿润的活性炭加入到粗TiCl4,目的是将AlCl3转化为Al(OH)3而除去
D.“还原”过程中还原剂可以选择金属钠,气氛可以选择N2