题目内容
6.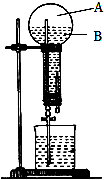 如图是做过氨气溶于水的喷泉实验装置,实验完成后烧瓶里的空间被分为两个部分:A和B,请根据实验内容按要求填空:
如图是做过氨气溶于水的喷泉实验装置,实验完成后烧瓶里的空间被分为两个部分:A和B,请根据实验内容按要求填空:(1)A中的主要成分是空气或N2、O2;
(2)B中溶液即为氨水,把酚酞滴入氨水中,溶液显红色,是因为NH3•H2O
 NH4++OH-(用离子方程式表示);
NH4++OH-(用离子方程式表示);(3)试剂的滴加顺序不同,有时会产生不同的现象.
①把氨水滴入Al2(SO4)3溶液中,②把Al2(SO4)3溶液滴入氨水中,①、②的实验现象是否相同相同(填“相同”或“不同”),写出反应①的化学方程式Al2(SO4)3+6NH3•H2O+6H2O=2Al(OH)3↓+3(NH4)2SO4;
反应②的离子方程式Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(4)把氨水滴加到FeSO4溶液中的现象为先生成白色沉淀,让后变成灰绿色,最后变成红褐色.
分析 (1)氨气极易溶于水,烧瓶内A为不溶于水的空气;
(2)氨气极易溶于水,与水反应生成一水合氨,一水合氨电离生成氨根离子与氢氧根离子,溶液显碱性;
(3)一水合氨为弱碱,与氢氧化铝不反应,铝离子与一水合氨反应生成氢氧化铝沉淀,据此判断现象,写出方程式;
把Al2(SO4)3溶液滴入氨水中反应实质铝离子与一水合氨反应生成氨根离子与氢氧化铝;
(4)硫酸亚铁与氨水反应生成氢氧化亚铁,氢氧化亚铁不稳定容易被氧气氧化生成氢氧化铁沉淀.
解答 解:(1)氨气极易溶于水,烧瓶内A为不溶于水的空气;
故答案为:空气或N2、O2;
(2)氨气极易溶于水,与水反应生成一水合氨,一水合氨电离生成氨根离子与氢氧根离子,离子方程式:NH3•H2O NH4++OH-,溶液显碱性,能够使酚酞变红色;
NH4++OH-,溶液显碱性,能够使酚酞变红色;
故答案为:红;NH3•H2O NH4++OH-;
NH4++OH-;
(3)①一水合氨为弱碱,与氢氧化铝不反应,所以把氨水滴入Al2(SO4)3溶液中或者把Al2(SO4)3溶液滴入氨水中,都生成氢氧化铝白色沉淀,反应①的化学方程式:Al2(SO4)3+6NH3•H2O+6H2O=2Al(OH)3↓+3(NH4)2SO4;
Al2(SO4)3溶液滴入氨水中反应实质铝离子与一水合氨反应生成氨根离子与氢氧化铝,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
故答案为:相同;Al2(SO4)3+6NH3•H2O+6H2O=2Al(OH)3↓+3(NH4)2SO4;Al3++3NH3•H2O=Al(OH)3↓+3NH4+;Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(4)硫酸亚铁与氨水反应生成白色的氢氧化亚铁沉淀,氢氧化亚铁不稳定容易被氧气氧化生成红褐色氢氧化铁沉淀,所以看到现象为:先生成白色沉淀,让后变成灰绿色,最后变成红褐色;
故答案为:先生成白色沉淀,让后变成灰绿色,最后变成红褐色.
点评 本题考查了喷泉实验,熟悉氨气的性质是解题关键,注意氢氧化铝与氢氧化亚铁的性质,题目难度中等.

 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案| A. | 盐酸 | B. | 氢氟酸 | C. | 烧碱 | D. | 饱和食盐水 |
| A. | 液化石油气和天然气的主要成分都是甲烷 | |
| B. | 糖类、脂类、蛋白质都属于天然高分子化合物 | |
| C. | 汽油、煤油、植物油均为含碳氢氧三种元素的化合物 | |
| D. | 误服重金属盐,立即服用牛奶或豆浆可解毒 |
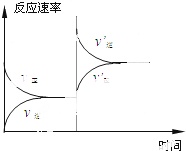
| A. | 加压 | B. | 增加O2的浓度 | ||
| C. | 使用催化剂 | D. | 同时增大SO3和O2的浓度 |
 氯原子对O3分解有催化作用:Cl+O3=ClO+O2△H1;ClO+O=Cl+O2△H2.大气臭氧层的分解反应是:O+O3=2O2△H,该反应的能量变化示意图如图:下列叙述中,正确的是( )
氯原子对O3分解有催化作用:Cl+O3=ClO+O2△H1;ClO+O=Cl+O2△H2.大气臭氧层的分解反应是:O+O3=2O2△H,该反应的能量变化示意图如图:下列叙述中,正确的是( )| A. | 反应O+O3=2O2的△H=E1-E3 | B. | O+O3=2O2是放热反应 | ||
| C. | △H=△H1+△H2 | D. | 反应O+O3=2O2的△H=E1-E2 |
| A. | 加工成饲料 | B. | 发酵后作农家肥 | C. | 就地焚烧 | D. | 制造沼气 |
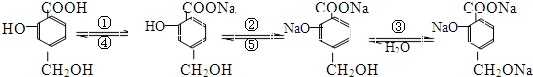

 ;
;