题目内容
18.对于平衡:2SO3(g)?2SO2(g)+O2(g)-Q(Q>0),符合右图变化情况的是( )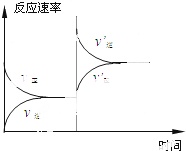
| A. | 加压 | B. | 增加O2的浓度 | ||
| C. | 使用催化剂 | D. | 同时增大SO3和O2的浓度 |
分析 该反应是一个反应前后气体体积增大、吸热的可逆反应,第一次达到平衡后,改变条件,正逆反应速率都增大,且逆反应速率大于正反应速率,说明平衡向逆反应方向移动,且改变条件时与原平衡点没有接触点.
解答 解:A.该反应是一个反应前后气体体积增大、吸热的可逆反应,增大压强,平衡向逆反应方向移动,且正逆反应速率都增大,再次达到平衡状态时,正逆反应速率都大于原来平衡反应速率,故A正确;
B.增加氧气浓度瞬间,能增大逆反应速率,但反应物浓度不变,所以正反应速率不变,应该与原来平衡点有接触点,所以不符合图象,故B错误;
C.催化剂能同等程度的改变正逆反应速率,只改变反应速率但不影响平衡移动,所以改变条件时正逆反应速率仍然相等,不符合图象,故C错误;
D.同时增大SO3和O2的浓度,正逆反应速率都增大,如果加入氧气浓度远远大于三氧化硫浓度,则平衡逆向移动,故D正确;
故选AD.
点评 本题以图象分析为载体考查外界条件对化学反应速率及化学平衡移动的影响,熟悉外界条件对反应速率及平衡移动影响原理是解本题关键,注意分析改变条件时与原平衡点是否接触,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
9.把CO2和NO的混合气体VL缓缓通过足量的Na2O2固体,充分反应后,测得剩余气体体积大约只有原来的一半,则混合气体中CO2和NO的体积比不可能是( )
| A. | 2:1 | B. | 3:2 | C. | 3:4 | D. | 5:4 |
13.经研究发现白蚁信息素有: (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),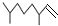 (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2) 8CH═CH-CH═CH(CH2)8CH3.下列说法不正确的是( )
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2) 8CH═CH-CH═CH(CH2)8CH3.下列说法不正确的是( )
 (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),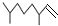 (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2) 8CH═CH-CH═CH(CH2)8CH3.下列说法不正确的是( )
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2) 8CH═CH-CH═CH(CH2)8CH3.下列说法不正确的是( )| A. | 2,4-二甲基-1-庚烯的分子式为C9H18 | |
| B. | 以上三种信息素均能使溴的四氯化碳溶液褪色 | |
| C. | 2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同系物 | |
| D. | 1 mol家蚕的性信息素与1 mol Br2加成,产物只有一种 |
3.氮的固定主要有三大途径,它们是生物固氮、大气固氮、工业固氮;氮肥主要有铵态氮肥、硝态氮肥和有机氮肥,目前氮肥中使用量最多的一种肥料是尿素;含氮、磷、钾三要素中的两种或两种以上的化学肥料称复合肥料.
10.下列有关热化学方程式及其叙述正确的是( )
| A. | 氢气的燃烧热为285.5 kJ•mol-1,则其燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-285.5 kJ•mol-1 | |
| B. | 已知2C(石墨,s)+O2(g)=2CO(g);△H=-221 kJ•mol-1,则石墨的燃烧热为110,5 kJ•mol-1 | |
| C. | 已知N2(g)+3H2(g)?2 NH3(g)△H=-92.4 kJ•mol-1,由于△H<0,故该反应一定能自发进行 | |
| D. | 热化学方程式中的化学计量数表示物质的量,可以是分数 |
8.下列关于能量变化的说法正确的是( )
| A. | 相同质量的水和冰相比较,冰的能量高 | |
| B. | 化学反应过程中能量的变化只有吸热和放热两种表现形式 | |
| C. | 化学反应既遵循质量守恒,也遵循能量守恒 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
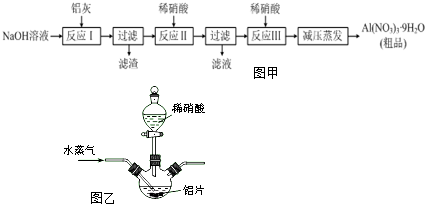
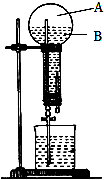 如图是做过氨气溶于水的喷泉实验装置,实验完成后烧瓶里的空间被分为两个部分:A和B,请根据实验内容按要求填空:
如图是做过氨气溶于水的喷泉实验装置,实验完成后烧瓶里的空间被分为两个部分:A和B,请根据实验内容按要求填空: NH4++OH-(用离子方程式表示);
NH4++OH-(用离子方程式表示);