题目内容
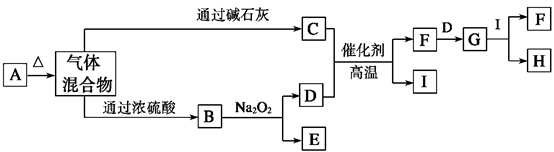
(10分)下图中A~I分别代表有关反应中的一种物质,其中A为酸式盐,请回答下列问题:
 (1)A、F的化学式分别为 、 。?
(1)A、F的化学式分别为 、 。?
(2)I的电子式为 ;I的沸点较高的原因是
(3)E的水溶液中,各离子浓度由大到小的顺序为
。
(4)写出反应B+Na2O2 → D+E的化学方程式:
(5)指出实验室中保存H的方法及其原因:
 (1)A、F的化学式分别为 、 。?
(1)A、F的化学式分别为 、 。?(2)I的电子式为 ;I的沸点较高的原因是
(3)E的水溶液中,各离子浓度由大到小的顺序为
。
(4)写出反应B+Na2O2 → D+E的化学方程式:
(5)指出实验室中保存H的方法及其原因:
(1)NH4HCO3 NO
(2)H O H? 存在分子间氢键
(3)c (Na+)>c(CO 32- )>c(OH-)>c(HCO 3- )>c(H+)
(4)2CO2+2Na2O2 =2Na2CO3+O2
(5)硝酸见光或受热容易分解,故通常保存在棕色瓶中并置于冷暗处
(2)H O H? 存在分子间氢键
(3)c (Na+)>c(CO 32- )>c(OH-)>c(HCO 3- )>c(H+)
(4)2CO2+2Na2O2 =2Na2CO3+O2
(5)硝酸见光或受热容易分解,故通常保存在棕色瓶中并置于冷暗处
本题是无机框图题,关键是找准突破点。框图中有两条重要信息:一是B经浓H2SO4干燥后可与过氧化钠反应,可以推知B可能为二氧化碳;二是A为酸式盐,加热后固体完全消失得到混合气体,可以推知A为弱酸酸式铵盐,则C为NH3,C与D能发生催化反应,故D为O2,E为Na2CO3。其余物质依次为A:NH4HCO3,F:NO,I:H2O,G:NO2。H:HNO。

练习册系列答案
相关题目