题目内容
10.下列说法中正确的是( )| A. | 升高温度,反应速率可能减小 | |
| B. | 需要加热的反应一定为吸热反应 | |
| C. | 使用催化剂不能使化学平衡发生移动 | |
| D. | 使某金属做电解池的阳极,可使该金属得到有效的保护 |
分析 A.升高温度,反应速率增大;
B.放热、吸热反应与是否加热无关;
C.催化剂同等程度改变反应速率;
D.金属为阳极,如不是惰性电极,易被氧化.
解答 解:A.升高温度,增大活化分子百分数,反应速率增大,故A错误;
B.放热、吸热反应与是否加热无关,如铝热反应为放热反应,但需要高温下进行,故B错误;
C.催化剂同等程度改变反应速率,加入催化剂只改变反应速率,平衡不移动,故C正确;
D.金属为阳极,如不是惰性电极,易被氧化,故D错误.
故选C.
点评 本题考查较为综合,涉及多角度的知识,为高考常见题型,侧重于学生的分析能力以及双基的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
20.下列说法正确的是( )
| A. | 按系统命名法,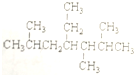 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次升高 | |
| C. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| D. | 2-甲基-1,3-丁二烯的键线式为 |
1.当燃烧8.96升由CH4、CO、C2H6组成的混和气体时,除生成水外,还生成17.92升CO2气体(气体体积均在标准状况下测定).则原混和气体中含C2H6的物质的量是( )
| A. | 0.2mol | B. | 0.4 mol | C. | 0.6 mol | D. | 0.8 mol |
18.下列实验操作正确的是( )
| A. | 将氢氧化钠固体放在滤纸上称量 | |
| B. | 用10 mL量筒量取8.58 mL蒸馏水 | |
| C. | 用强光照射鉴别淀粉胶体与碳酸钠两种无色液体 | |
| D. | 蒸馏时,应将温度计的水银球插入液面以下 |
5.将下列固体溶于水,再将其溶液加热蒸发,结晶后再灼烧,能得到化学组成与原固体物质相同的是( )
①胆矾 ②氯化铝 ③硫酸铝 ④碳酸钠 ⑤碳酸氢钠 ⑥氯化铜.
①胆矾 ②氯化铝 ③硫酸铝 ④碳酸钠 ⑤碳酸氢钠 ⑥氯化铜.
| A. | ③④ | B. | ①③④ | C. | ①②③④⑤ | D. | 全部 |
15.为达到预期的实验目的,下列操作正确的是( )
| A. | 向无色溶液中加BaCl2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,由此确定该溶液中一定含有SO${\;}_{4}^{2-}$ | |
| B. | 用pH试纸测定氯水的pH | |
| C. | 欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 | |
| D. | 为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 |
2.含有M金属的铁5.6克,与足量稀硫酸反应,得到氢气0.56克,则金属M可能是( )
| A. | Mg | B. | Al | C. | Zn | D. | Cu |
