题目内容
5.将下列固体溶于水,再将其溶液加热蒸发,结晶后再灼烧,能得到化学组成与原固体物质相同的是( )①胆矾 ②氯化铝 ③硫酸铝 ④碳酸钠 ⑤碳酸氢钠 ⑥氯化铜.
| A. | ③④ | B. | ①③④ | C. | ①②③④⑤ | D. | 全部 |
分析 将固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同,说明该物质较稳定,加热不分解,且不水解生成挥发性酸,据此分析解答.
解答 解:①胆矾溶于水后,将溶液蒸发结晶再灼烧得到硫酸铜而不是胆矾,所以得不到原物质,故错误;
②氯化铝溶于水后,将溶液蒸发结晶时促进氯化铝水解,氯化氢具有挥发性,所以蒸发结晶得到的固体是氢氧化铝,再灼烧氢氧化铝得到氧化铝,所以得不到原物质,故错误;
③硫酸铝溶于水后,蒸发过程中硫酸铝水解得到硫酸和氢氧化铝,但硫酸没有挥发性,所以蒸发结晶得到的固体是硫酸铝,硫酸铝较稳定,在灼烧时不分解,所以最终得到的固体是原物质,故正确;
④纯碱溶于水后,蒸发结晶过程中得到的固体是碳酸钠,碳酸钠较稳定,加热时不分解,所以最终得到原物质,故正确;
⑤小苏打溶于水后,蒸发结晶过程中得到的固体是碳酸钠,所以得不到原物质,故错误;
⑥氯化铜溶于水后,蒸发结晶过程中氯化铜水解生成氢氧化铜和氯化氢,蒸发促进氯化氢挥发,所以蒸发结晶得到的固体是氢氧化铜,氢氧化铜不稳定,在灼烧时分解生成氧化铜,所以最终得到的固体不是原物质,故错误;
故选A.
点评 本题以盐类水解为载体考查物质的性质,只有性质稳定、水解不生成挥发性酸的盐蒸发结晶得到原来物质,水解生成挥发性酸的盐蒸发结晶灼烧时得到氧化物,题目难度中等.

练习册系列答案
相关题目
15.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 将1 mol Cl2通入H20中,生成NA个HC10分子 | |
| B. | 32 g硫在空气中燃烧,该反应转移6NA个电子 | |
| C. | 标准状况下,2.24 L CO气体中约含有1.4NA个质子 | |
| D. | 室温下,1 L pH=3的H2S04,溶液中,H2S04,电离出2×10 -3 NA个H+ |
16.有A、B、C、D、E五种前四周期元素,其元素特征信息如表:
回答下列问题:
(1)元素C在周期表中的位置为第3周期ⅠA族.
(2)B基态原子的核外电子排布图 ;E基态原子的电子排布式1s22s22p63s23p63d54s1.
;E基态原子的电子排布式1s22s22p63s23p63d54s1.
(3)写出化合物A2B2的电子式 .
.
(4)D的氢氧化物与化合物CBA反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(5)B与C(碳)、N(氮)相比,第一电离能由大到小的顺序为N>O>C.
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,电离能(I)数据依次为:I1=490kJ/mol-1,I2=4562kJ/mol-1,I3=6912kJ/mol-1… |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 在第四周期元素原子中,其所含不成对电子数最多 |
(1)元素C在周期表中的位置为第3周期ⅠA族.
(2)B基态原子的核外电子排布图
 ;E基态原子的电子排布式1s22s22p63s23p63d54s1.
;E基态原子的电子排布式1s22s22p63s23p63d54s1.(3)写出化合物A2B2的电子式
 .
.(4)D的氢氧化物与化合物CBA反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(5)B与C(碳)、N(氮)相比,第一电离能由大到小的顺序为N>O>C.
13.下列有关化学反应速率的说法正确的是( )
| A. | 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 | |
| B. | 100 mL 2 mol•L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| C. | SO2的催化氧化是一个放热反应,升高反应的温度,反应速率减慢 | |
| D. | 用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率 |
10.下列说法中正确的是( )
| A. | 升高温度,反应速率可能减小 | |
| B. | 需要加热的反应一定为吸热反应 | |
| C. | 使用催化剂不能使化学平衡发生移动 | |
| D. | 使某金属做电解池的阳极,可使该金属得到有效的保护 |
17.下列微粒中:①12Mg2+ ②Na2-③ ④O2-,核外电子总数相同的是( )
④O2-,核外电子总数相同的是( )
 ④O2-,核外电子总数相同的是( )
④O2-,核外电子总数相同的是( )| A. | ②③④ | B. | ①②④ | C. | ①②③ | D. | ①③④ |
20.下列过程不发生化学变化的是( )
| A. | 石油的分馏 | B. | 煤的干馏 | ||
| C. | 以海水为原料获取单质溴 | D. | 蛋白质溶液中滴加硫酸铜 |
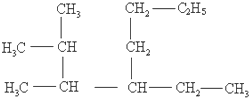 (1)3-甲基-2-乙基-1-丁烯的结构简式:
(1)3-甲基-2-乙基-1-丁烯的结构简式: