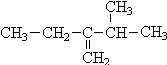题目内容
4.镁是海水中含量较多的金属,镁合金及其镁的化合物用途非常广泛.
(1)Mg2Ni是一种储氢合金,已知:
Mg(s)+H2(g)=MgH2(S)△H1=-74.5kJ•mol-1
Mg2Ni(s)+2H2(g)=Mg2NiH4(s)△H2=-64.4kJ•mol-l
则:Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)的△H3=+84.6KJ/mol.
(2)某科研小组用水氯镁石(主要成分为MgCl2•6H2O)制备金属镁工艺的关键流程如图1:
科研小组将MgCl2•6H2O在氩气气氛中进行热重分析,结果如图2(TG表示残留固体质量占原样品总质量的百分数).
①图中AB线段为“一段脱水”,试确定B点对应固体物质的化学式MgCl2•2H2O;图中BC线段为“二段脱水”,在实验中通入H2和Cl2燃烧产物的目的是抑制MgCl2的水解.
②该工艺中,可以循环使用的物质有HCl,Cl2.
(3)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是+2,该化合物水解时生成甲烷、氯化镁和氢氧化镁,请写出该反应的化学方程式2CH3MgCl+2H2O=Mg(OH)2+MgCl2+2CH4↑.
(4)储氢材料Mg(AIH4)2在110~200℃的反应为:Mg(AIH4)2=MgH2+2Al+3H2↑;每转移3mol电子生成Al的质量为27g.
(5)“镁次氯酸盐”燃料电池的装置如图3所示,该电池的正极反应式为ClO-+2e-+H2O=Cl-+2OH-.
分析 (1)依据热化学方程式①Mg(s)+H2(g)=MgH2(S)△H1=-74.5kJ•mol-1;②Mg2Ni(s)+2H2(g)=Mg2NiH4(s)△H2=-64.4kJ•mol-l,利用盖斯定律将②-2×①得到反应Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s),进而计算反应热;
(2)①图中AB线段为“一段脱水”,设B点对应固体物质的化学式为MgCl2•xH2O,根据$\frac{18x+95}{6×18+95}$=0.645,可计算确定B的化学式;二段脱水中通入HCl可以抑制MgCl2的水解;
②制备金属镁工艺的关键流程分析,循环使用的物质是加入后在反应过程中有重新生成分析判断;
(3)根据化合价代数和为0判断镁的化合价,根据元素守恒书写化学方程式;
(4)根据氧化还原反应Mg(AIH4)2=MgH2+2Al+3H2↑中电子转移数目与产物的物质的关系进行计算;
(5)依据“镁-次氯酸盐”燃料电池的装置图中所示,原电池的正极应发生还原反应,元素的化合价降低,根据图示可知,正极上是ClO-变为Cl-,据此写出正极反应式.
解答 解:(1)①Mg(s)+H2(g)═MgH2(s)△H1=-74.5kJ•mol-1
②Mg2Ni(s)+2H2(g)═Mg2NiH4(s)△H2=-64.4kJ•mol-1
Mg2Ni(s)+2MgH2(s)═2Mg(s)+Mg2NiH4(s)△H3
由盖斯定律②-2×①得到Mg2Ni(s)+2MgH2(s)═2Mg(s)+Mg2NiH4(s)△H3 =-64.4KJ/mol-2×(-74.5KJ/mol)=+84.6KJ/mol,则△H3=+84.6KJ/mol,
故答案为:+84.6KJ/mol;
(2)①图中AB线段为“一段脱水”,设B点对应固体物质的化学式为MgCl2•xH2O,根据$\frac{18x+95}{6×18+95}$=0.645,计算得 x=2,所以B的化学式为MgCl2•2H2O;二段脱水中通入HCl可以抑制MgCl2的水解,
故答案为:MgCl2•2H2O;抑制MgCl2的水解;
②制备金属镁工艺的关键流程分析,循环使用的物质是加入后在反应过程中有重新生成的物质,分析可知是氯气和氯化氢,
故答案为:HCl,Cl2;
(3)根据CH3MgCl中各元素化合价代数和为0可知镁的化合价为+2价,CH3MgCl水解时生成甲烷、氯化镁和氢氧化镁,反应的化学方程式为2CH3MgCl+2H2O=Mg(OH)2+MgCl2+2CH4↑,
故答案为:+2;2CH3MgCl+2H2O=Mg(OH)2+MgCl2+2CH4↑;
(4)储氢材料Mg(AlH4)2在110℃-200℃的反应为:Mg(AlH4)2=MgH2+2Al+3H2↑,反应中生成2molAl转移电子6mol,所以每转移3mol电子生成Al的物质的量为1mol,即质量为27g,
故答案为:27g;
(5)“镁-次氯酸盐”燃料电池的装置图中微粒变化分析可知,ClO-在正极放电,生成Cl-,结合碱性的环境,可写出正极反应式:ClO-+2e-+H2O=Cl-+2OH-,
故答案为:ClO-+2e-+H2O=Cl-+2OH-.
点评 本题考查了热化学方程式书写方法,物质制备实验的分析判断,原电池原理和电极原理的分析应用,图象分析能力,掌握基础知识是关键,题目难度中等.

| A. | 用润湿的pH试纸测定0.1mol/L氨水的pH值 | |
| B. | 在CaCO3饱和溶液中,加入Na2CO3固体,平衡时c(Ca2+)=c(CO${\;}_{3}^{2-}$)=$\sqrt{{K}_{sp}CaC{O}_{3}}$ | |
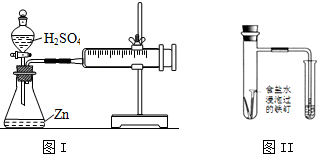
| C. | 图I装置可用于探究浓度对化学反应速率的影响 | |
| D. | 观察图II导管中水柱的变化,可知该条件下铁钉主要发生了析氢腐蚀 |
| A. | 升高温度,反应速率可能减小 | |
| B. | 需要加热的反应一定为吸热反应 | |
| C. | 使用催化剂不能使化学平衡发生移动 | |
| D. | 使某金属做电解池的阳极,可使该金属得到有效的保护 |
N2(g)+2O2(g)=N2O4(g)△H=+8.7kJ•mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534.0kJ•mol-1
下列表示肼跟N2O4反应的热化学方程式,正确的是( )
| A. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-542.7 kJ•mol-1 | |
| B. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1059.3 kJ•mol-1 | |
| C. | N2H4(g)+$\frac{1}{2}$N2O4(g)=$\frac{3}{2}$N2(g)+2H2O(g)△H=-1076.7 kJ•mol-1 | |
| D. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1076.7 kJ•mol-1 |
| 物质 | A | B | C |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 发生的反应可表示为A+3B?2C | |
| B. | 反应达到平衡时B的转化率为25% | |
| C. | 若起始时密闭容器中0.1molA,0.1molB,0.2molC时,反应达到平衡时,c(A)=0.05mol•L-1 | |
| D. | 改变起始时容器中各气体的物质的量,可以改变此反应的平衡常数 |
| A. | 5、5、10、10 | B. | 4、4、10、10 | C. | 3、5、11、9 | D. | 5、3、9、11 |
| 实验方案 | 试验现象 |
| 1 用砂纸打磨后的镁条与沸水反应,再向反应溶液中滴加酚酞 2 向Na2S 饱和溶液中滴加新制的氯水 3 钠与滴有酚酞的冷水反应 4 镁条与amol/L的盐酸反应 5 铝片与amol/L的盐酸反应 6 向AlCl3溶液中滴加NaOH,至过量 | Ⅰ浮于水面,熔成小球,四处游动,逐渐缩小,溶液变红 Ⅱ放出无色气体,气体可燃,溶液变浅红色Ⅲ反应不是很剧烈,产生的气体可燃 Ⅳ剧烈反应,产生的气体可燃 Ⅴ先生成白色絮状沉淀,继而沉淀消失 Ⅵ生成淡黄色沉淀 |
(1)该同学的试验目的为:第三周期元素性质递变规律.
(2)请根据实验记录表,填写试验现象序号对应的试验方案编号:
Ⅰ3,Ⅱ1,Ⅲ5,Ⅳ4.
(3)请分别写出下列实验方案中,各现象对应的离子方程式:
试验方案2:Cl2+H2S=S↓+2H++2Cl-;
试验方案6:Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O或(Al3++4OH-=AlO2-+2H2O).
(4)试验结论是:第三周期元素随原子序数的增大,元素的金属性逐渐减弱,非金属性逐渐增强.
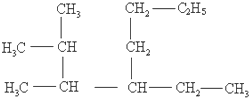 (1)3-甲基-2-乙基-1-丁烯的结构简式:
(1)3-甲基-2-乙基-1-丁烯的结构简式: