题目内容
7.为测定某有机化合物A的结构,进行如下实验.【分子式的确定】
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下).则该物质中各元素的原子个数比是n(C):n(H):n(O)=2:6:1;
(2)质谱仪测定定机化合物的相对分子质量为46,则该物质的分子式是C2H6O;
(3)根据价键理论,预测A的可能结构并写出结构简式①CH3CH2OH②CH3-O-CH3.
【结构式的确定】
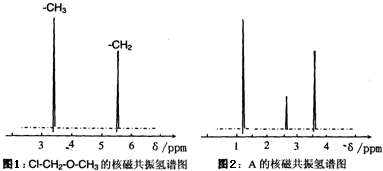
(4)核磁共振氢原子光谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl-CH2-O-CH3)有两种氢原子(图1).经测定,有机物A的核磁共振氢谱示意图如图2,则A的结构简式为CH3CH2OH.
【性质实验】
(5)A在一定条件下脱水可生成B,B可合成包装塑料C,请写出B转化为C的化学反应方程式:
 .
.(6)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉.请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,请写出制备反应方程式:nCH2=CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl.
(7)A可通过粮食在一定条件下制得,由粮食制得的A在一定温度下密闭储存,因为发生一系列的化学变化而变得更醇香.请写出最后一步反应的化学方程式:C2H5OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
分析 本题考查了研究有机物的一般步骤和方法,
(1)利用燃烧生成的二氧化碳和水可以推出有机物的实验式(即最简式)C2H6O;
(2)利用分子量可以进一步推出分子式C2H6O;
(3)根据价键理论,推导出可能的结构式①CH3CH2OH②CH3-O-CH3;
(4)利用核磁共振氢谱(可以读出氢原子的种类和个数比),推出有机物的真实结构即可;
(5)乙烯可以发生加聚反应的得到聚乙烯塑料;
(6)乙烯可以和氯化氢之间发生加成反应得到氯乙烷;
(7)乙醇发酵可以得到乙酸,乙酸和乙醇之间可以发生酯化反应得到乙酸乙酯和水,酯具有香味.
解答 解:(1)5.4克水为0.3mol,含氢原子0.6mol、氧原子0.3mol,8.8克二氧化碳为0.2mol,含碳原子0.2mol、氧原子0.4mol,消耗氧气6.72L为0.3mol即氧原子0.6mol,所以有机物中含氧原子0.3+0.4-0.6=0.1mol,该物质中各元素的原子个数比n(C):n(H):n(O)=0.2:0.6:0.1=2:6:1
故答案为:n(C):n(H):n(O)=2:6:1;
(2)( C2H6O)x 相对分子质量为46,解得x=1,
故答案为:C2H6O;
(3)根据价键理论:碳周围四个键,氧周围两个键,氢周围一个键,得A:C2H6O的可能结构为:①CH3CH2OH ②CH3-O-CH3,故答案为:①CH3CH2OH ②CH3-O-CH3;
(4)有机物A的核磁共振氢谱示意图知该有机物中有3种氢且个数比为1:2:3,则A的结构简式为CH3CH2OH;
故答案为:CH3CH2OH;
(5)A在一定条件下脱水可生成B,B可合成包装塑料C,知A为乙醇、脱水后生成B乙烯,乙烯可以发生加聚反应得到聚乙烯,则C为聚乙烯.
故答案为: ;
;
(6)原子利用率为100%故应用加成反应,乙烯可以和氯化氢之间发生加成反应得到氯乙烷,即CH2=CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl;
故答案为,nCH2=CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl;
(7)乙醇可通过粮食在一定条件下制得,由粮食制得的乙醇在一定温度下密闭储存,因为发生一系列的化学变化,得到乙酸乙酯而变得更醇香,最后一步反应的化学方程式C2H5OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,故答案为:C2H5OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
点评 本题考查比较综合,关键是有机物的推断,燃烧法做题推导有机物的结构,进而进一步应用解决题目,难度中等.

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案| A. | 向溴水中通入某气体,溴水颜色褪去,说明该气体一定是乙烯 | |
| B. | 向海鲜浸出液中加入新制氢氧化铜,加热,产生红色沉淀,说明浸出液中可能含甲醛 | |
| C. | 向溴乙烷中直接加入硝酸银溶液,无浅黄色沉淀生成,说明该溴乙烷已变质 | |
| D. | 向蛋清中滴加CuSO4溶液,有固体析出,加水固体不溶解,说明蛋白质发生变性 |
| A. | 对泄露的苯酚用石灰水中和比用酒精冲洗掉的方法好 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升髙而增大,超过65℃可以与水以任意比互溶 | |
| D. | 碳酸氢钠溶液中滴人苯酚的水溶液后会放出二氧化碳 |
| A. | 玻璃、陶瓷、水泥属于无机硅酸盐材料,其生产原料都是石灰石 | |
| B. | 钢铁里的铁和碳在潮湿的空气中因构成许多原电池而易发生电化学腐蚀 | |
| C. | 聚氯乙烯塑料在日常生活中可用来进行食品包装 | |
| D. | 铝制品在空气中不易被腐蚀,是因为常温下铝不与氧气反应 |
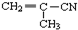 ②
②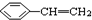 ③
③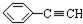 ④CH3-CH=CH-CN ⑤CH2=CH-CH=CH2,其中可用于合成高分子材料(结构如图所示)的正确组合为( )
④CH3-CH=CH-CN ⑤CH2=CH-CH=CH2,其中可用于合成高分子材料(结构如图所示)的正确组合为( )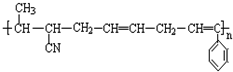
| A. | ①②④ | B. | ①②⑤ | C. | ②④⑤ | D. | ③④⑤ |
| A. | 乙醛、乙酸 | B. | 甲酸乙酯、丙酸 | ||
| C. | CH3CH2CHO、CH3COCH3 | D. | CH3CH2CH2OH、CH3OCH2CH3 |

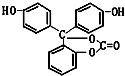 如图所示下列物质最多与5molNaOH反应,最多与4molBr2反应,最多与9molH2反应.它的分子式为C20H14O5.
如图所示下列物质最多与5molNaOH反应,最多与4molBr2反应,最多与9molH2反应.它的分子式为C20H14O5.