��Ŀ����
20��ij���{�ٹ�·�������Ӳ۹�й©�¹ʣ����²��ֱ���й©�������Ⱦ�����ж��ڱ��ӵ������У�������ǣ�������| A�� | ��й¶�ı�����ʯ��ˮ�кͱ��þƾ���ϴ���ķ����� | |
| B�� | ��Ũ��Һ��Ƥ����ǿ�ҵĸ�ʴ�ԣ��������մ��Ƥ���ϣ�Ӧ�����þƾ���ϴ | |
| C�� | ����ˮ�е��ܽ�����¶ȵ����{��������65�������ˮ������Ȼ��� | |
| D�� | ̼��������Һ�е��˱��ӵ�ˮ��Һ���ų�������̼ |
���� A���ƾ����ӷ����Ҽ۸�ϸߣ���ʯ��ˮ�ܹ��뱽�ӷ����кͷ�Ӧ���Ҽ۸��ʵ�ݣ�
B�����������ھƾ��������þƾ�ϴ��ճ��Ƥ���ϵı��ӣ�
C���ƾ�����ˮ���ܽ�Ƚ�С�������¶ȸ���65�����ˮ������Ȼ��ܣ�
D����������С��̼�����ԣ��������ɶ�����̼���壮
��� �⣺A�����ھƾ����ӷ����Ҽ۸�ϸߣ���ʯ��ˮ�ܹ��뱽�ӷ����кͷ�Ӧ���Ҽ۸��ʵ�ݣ����Զ�й¶�ı�����ʯ��ˮ�кͱ��þƾ���ϴ���ķ����ã���A��ȷ��
B�������ж�����������ˮ�������ھƾ�������Ũ��Һ����մ��Ƥ���ϣ�Ӧ�����þƾ���ϴ����B��ȷ��
C��������ˮ�е��ܽ�����¶ȵ����߶���������65�������ˮ������Ȼ��ܣ���C��ȷ��
D�����ڱ�������С��̼�����ԣ���̼��������Һ�е��뱽�ӵ�ˮ��Һ���������ɶ�����̼���壬��D����
��ѡD��
���� ���⿼��ѧ�����ӵ����ʣ���Ŀ�ѶȲ���ע�����ձ��ӵ����ʼ���Ӧ�ã���ȷ������̼�ᡢ̼��������ӵ�����ǿ����������ػ���֪ʶ�Ŀ��飬������ѧ�����Ӧ�û���֪ʶ��������

��ϰ��ϵ�д�
�����Ŀ
10����������֮���ת��������һ��ʵ�ֵ��ǣ�������
| A�� | Na2O��NaOH | B�� | NaHCO3��Na2CO3 | C�� | SiO2��H2SiO3 | D�� | NH3��NO |
11������ʽΪC10H14�ķ������������ķ�����ֻ��һ�����������Һ���ڴ������ڵ������·�Ӧ�����ɱ����ϵ�һ�����Ľṹ��12 �֣��������Ľṹ�У�������
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
8�������л���Ӧ�ķ���ʽ��д������ǣ�������
| A�� | CH4+Cl2$\stackrel{����}{��}$CH3Cl+HC1 | B�� | 2CH3CH2OH+02$\stackrel{Cu����}{��}$2CH3CH0+2H20 | ||
| C�� | 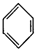 +HNO3$��_{50-60��}^{Ũ����}$ +HNO3$��_{50-60��}^{Ũ����}$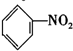 +H2O +H2O | D�� | nCH2=CH2$\stackrel{һ������}{��}$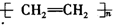 |
15��X��Y��Z��Ϊ������Ԫ�أ�X��Y����ͬһ���ڣ�X��Z����ͼ����ӷֱ�ΪX2-��Z-��Y+��Z-������ͬ�ĵ��Ӳ�ṹ������˵����ȷ���ǣ�������
| A�� | ԭ��������������X��Y��Z | B�� | ԭ��������X��Y��Z | ||
| C�� | ���ʷе㣺Z��Y��X | D�� | ���Ӱ뾶��X2-��Y+��Z- |
5��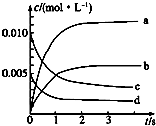 ��2L�ܱ������ڣ�800��ʱ��Ӧ2NO��g��+O2��g���T2NO2��g����ϵ�У�n��NO����ʱ��ı仯���±���
��2L�ܱ������ڣ�800��ʱ��Ӧ2NO��g��+O2��g���T2NO2��g����ϵ�У�n��NO����ʱ��ı仯���±���
��1����ͼ��ʾNO2��Ũ�ȱ仯��������b����O2��ʾ��0��2s�ڸ÷�Ӧ��ƽ������v=1.5��10-3mol•L-1•s-1��
��2����˵���÷�Ӧ�Ѵﵽƽ��״̬����bc��
a��v��NO2��=2v��O2�� b��������ѹǿ���ֲ���
c��v����NO��=2v����O2�� d���������ܶȱ��ֲ��䣮
 ��2L�ܱ������ڣ�800��ʱ��Ӧ2NO��g��+O2��g���T2NO2��g����ϵ�У�n��NO����ʱ��ı仯���±���
��2L�ܱ������ڣ�800��ʱ��Ӧ2NO��g��+O2��g���T2NO2��g����ϵ�У�n��NO����ʱ��ı仯���±���| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO��/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��2����˵���÷�Ӧ�Ѵﵽƽ��״̬����bc��
a��v��NO2��=2v��O2�� b��������ѹǿ���ֲ���
c��v����NO��=2v����O2�� d���������ܶȱ��ֲ��䣮
 ��
��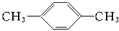 ��
�� CH3COOCH2CH3+H2O��
CH3COOCH2CH3+H2O��
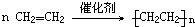 ��
��