题目内容
13.下列除杂质的方法不可行的是( )| A. | 除去NaHCO3溶液中少量的Na2CO3:通入过量的CO2 | |
| B. | 除去MgCl2溶液中少量的AlCl3:加入过量氢氧化钠溶液,过滤,用蒸馏水洗涤沉淀后用稀盐酸溶解沉淀 | |
| C. | 除去K2CO3固体中少量NaHCO3:置于坩埚中加热 | |
| D. | 用盐酸除去AgCl中少量的Ag2CO3 |
分析 A、碳酸钠和二氧化碳、水反应生成碳酸钠;
B、加入过量氢氧化钠溶液,Al3+生成偏铝酸根,过滤得到氢氧化镁沉淀,加盐酸溶沉淀解,得到氯化镁;
C、加热NaHCO3生成Na2CO3;
D、盐酸和碳酸银反应生成氯化银、二氧化碳和水.
解答 解:A、碳酸钠和二氧化碳、水反应生成碳酸钠,把杂质转化为NaHCO3溶液的溶质,故A正确;
B、加入过量氢氧化钠溶液,Al3+生成偏铝酸根,过滤得到氢氧化镁沉淀,加盐酸溶解沉淀,得到氯化镁,故B正确;
C、加热NaHCO3生成Na2CO3,仍然是K2CO3固体的杂质,故C错误;
D、盐酸和碳酸银反应生成氯化银、二氧化碳和水,除去了碳酸银,故D正确;
故选C.
点评 本题考查了除杂操作的基本原则,以及钠的重要化合物的化学性质,难度不大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
4.X、Y、Z、W是四种短周期元素,有关它们的信息如下表所示.
请回答下列问题:
(1)X的单质分子X2的结构式是S=S.
(2)X、Y、Z三元素的最高价氧化物对应水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2CO3(用化学式表示).
(3)常温时,W的硫酸盐溶液的pH<(填“=”、“>”或“<”)7,理由是Al3++3H2O?Al(OH)3+3H+(用离子方程式表示).
(4)25℃、101kPa时,32g Y的最简单气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol.
| 元素 | 部分结构知识 | 部分性质 |
| X | X原子核外电子占有9个原子轨道 | X的一种氧化物是形成酸雨的主要物质 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
(1)X的单质分子X2的结构式是S=S.
(2)X、Y、Z三元素的最高价氧化物对应水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2CO3(用化学式表示).
(3)常温时,W的硫酸盐溶液的pH<(填“=”、“>”或“<”)7,理由是Al3++3H2O?Al(OH)3+3H+(用离子方程式表示).
(4)25℃、101kPa时,32g Y的最简单气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol.
1.用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 在1 mol•L-1的KClO3溶液中,K+的个数为NA | |
| B. | 在标准状况下,22.4 L CH3CH2OH的分子数为NA | |
| C. | 32 g氧气和臭氧的混和气体中含有的氧原子数为2NA | |
| D. | 22.4 L HCl气体中含有的分子数为NA |
8.将30mL 5mol/L NaOH溶液加水稀释到60mL,稀释后溶液中NaOH的物质的量为( )
| A. | 0.25mol | B. | 2.5mol | C. | 0.15mol | D. | 1.5mol |
18.下列关于热化学反应的描述中正确的是( )
| A. | HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566.0 kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | Ba(OH)2•8H2O与NH4Cl反应的焓变小于0,所以在常温下能自发进行 |
2.下列变化不需要破坏化学键的是( )
| A. | HCl气体溶于水 | B. | 碘晶体受热转变成碘蒸气 | ||
| C. | NaCl溶于水 | D. | 加热HI气体使之分解 |
 .
.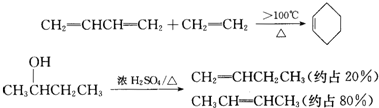

 ;C
;C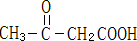 ;D
;D .
.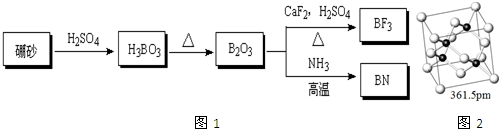
 ,BN中B元素的化合价为+3;
,BN中B元素的化合价为+3; ,其二氯代物有4种.
,其二氯代物有4种.