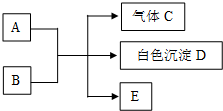
题目内容
4.X、Y、Z、W是四种短周期元素,有关它们的信息如下表所示.| 元素 | 部分结构知识 | 部分性质 |
| X | X原子核外电子占有9个原子轨道 | X的一种氧化物是形成酸雨的主要物质 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
(1)X的单质分子X2的结构式是S=S.
(2)X、Y、Z三元素的最高价氧化物对应水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2CO3(用化学式表示).
(3)常温时,W的硫酸盐溶液的pH<(填“=”、“>”或“<”)7,理由是Al3++3H2O?Al(OH)3+3H+(用离子方程式表示).
(4)25℃、101kPa时,32g Y的最简单气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol.
分析 X、Y、Z、W是短周期的四种元素,X原子核外电子占有9个原子轨道,核外电子填充1s、2s、2p、3s、3p轨道,且X的一种氧化物是形成酸雨的主要物质,故X为硫元素;
Y原子的次外层电子数等于最外层电子数的一半,则Y有2个电子层,最外层电子数为4,故Y为碳元素;
Z原子的最外层电子数多于4,Z元素的最高正化合价与最低负化合价代数和等于6,最外层电子数为7,故Z为Cl元素;
W原子的最外层电子数等于2n-3(n为原子核外电子层数),化学反应中W原子易失去最外层电子形成Wn+,W为金属元素,最外层电子数为n,故2n-3=n,故n=3,故W为Al元素,据此进行解答.
解答 解:X、Y、Z、W是短周期的四种元素,X原子核外电子占有9个原子轨道,核外电子填充1s、2s、2p、3s、3p轨道,且X的一种氧化物是形成酸雨的主要物质,故X为硫元素;Y原子的次外层电子数等于最外层电子数的一半,则Y有2个电子层,最外层电子数为4,故Y为碳元素;Z原子的最外层电子数多于4,Z元素的最高正化合价与最低负化合价代数和等于6,最外层电子数为7,故Z为Cl元素;W原子的最外层电子数等于2n-3(n为原子核外电子层数),化学反应中W原子易失去最外层电子形成Wn+,W为金属元素,最外层电子数为n,故2n-3=n,故n=3,故W为Al元素,
(1)X为硫元素,分子式为X2的单质为S2,S2电子式为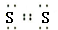 ,则其结构式为:S=S,故答案为:S=S;
,则其结构式为:S=S,故答案为:S=S;
(2)由于非金属性:Cl>S>C,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则有酸性:HClO4>H2SO4>H2CO3,
故答案为:HClO4>H2SO4>H2CO3;
(3)含W的一种硫酸盐是常用的净水剂,为Al2(SO4)3,硫酸铝溶液中铝离子水解:Al3++3H2O?Al(OH)3+3H+,溶液pH<7,
故答案为:<;Al3++3H2O?Al(OH)3+3H+;
(4)Y的最简单气态氢化物为CH4,25℃、101kPa时,32gCH4的物质的量为:$\frac{32g}{16g/mol}$=2mol,完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,1mol甲烷完全燃烧放出的热量为1780.6kJ×$\frac{1mol}{2mol}$=890.3kJ,故该反应的热化学反应方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol,
故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol.
点评 本题考查位置、结构与性质关系的综合应用,题目难度中等,涉及热化学方程式书写、常用化学用语、盐类水解等知识,题目难度中等,推断元素是解答关键,(1)中的S2的结构判断,结合氧气的结构分析.

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案| A. | H2→H2O | B. | H+→H2 | C. | HClO→HCl | D. | ClO3-→Cl- |
| A. | 11种 | B. | 12种 | C. | 13种 | D. | 14种 |
| A. | vA=0.05mol/(L•s) | B. | vB=0.03mol/(L•s) | C. | vC=3.6mol/(L•min) | D. | vD=0.1mol/(L•s) |
| A. | 除去NaHCO3溶液中少量的Na2CO3:通入过量的CO2 | |
| B. | 除去MgCl2溶液中少量的AlCl3:加入过量氢氧化钠溶液,过滤,用蒸馏水洗涤沉淀后用稀盐酸溶解沉淀 | |
| C. | 除去K2CO3固体中少量NaHCO3:置于坩埚中加热 | |
| D. | 用盐酸除去AgCl中少量的Ag2CO3 |
| A. | 乙烯可作水果的催熟剂 | |
| B. | 甘油可用于护肤用品 | |
| C. | 料酒可以除去食物中的腥味 | |
| D. | 裂化汽油可用作提取碘水中碘的萃取剂 |