题目内容
1.用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )| A. | 在1 mol•L-1的KClO3溶液中,K+的个数为NA | |
| B. | 在标准状况下,22.4 L CH3CH2OH的分子数为NA | |
| C. | 32 g氧气和臭氧的混和气体中含有的氧原子数为2NA | |
| D. | 22.4 L HCl气体中含有的分子数为NA |
分析 A、溶液体积不明确;
B、标况下,乙醇为液态;
C、氧气和臭氧均由氧原子构成;
D、HCl气体所处的状态不明确.
解答 解:A、溶液体积不明确,故溶液中的钾离子的个数无法计算,故A错误;
B、标况下,乙醇为液态,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、氧气和臭氧均由氧原子构成,则32g混合气体中含有的氧原子的物质的量n=$\frac{32g}{16g/mol}$=2mol,即2NA个,故C正确;
D、HCl气体所处的状态不明确,不一定是标况,故含有的分子数无法确定,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,根据物质的结构和公式来计算,难度不大.

练习册系列答案
 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案
相关题目
11.某溶液含有CO32-、HCO3-、S2-、CH3COO-、PO43-五种阴离子.向上述溶液中加入过量盐酸后,上述阴离子数目会减少的是( )
| A. | CO32-和HCO3- | B. | CO32-,HCO3-和S2- | ||
| C. | CO32-,HCO3-,S2-,CH3COO- | D. | 全部 |
12.芳香族化合物C8H9Cl的同分异构体有( )
| A. | 11种 | B. | 12种 | C. | 13种 | D. | 14种 |
16.在2A(g)+B(g)?3C(g)+4D(g)反应中,表示该反应速率最快的是( )
| A. | vA=0.05mol/(L•s) | B. | vB=0.03mol/(L•s) | C. | vC=3.6mol/(L•min) | D. | vD=0.1mol/(L•s) |
6.能正确表示下列反应的离子方程式为( )
| A. | 硫化亚铁溶于稀硝酸中:FeS+2H+═Fe2++H2S↑ | |
| B. | 含等物质的量的KHCO3和Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| C. | 少量CO2通入硅酸钠溶液中:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3- | |
| D. | 硫化钠水溶液呈碱性:S2-+2H2O?H2S+2OH- |
13.下列除杂质的方法不可行的是( )
| A. | 除去NaHCO3溶液中少量的Na2CO3:通入过量的CO2 | |
| B. | 除去MgCl2溶液中少量的AlCl3:加入过量氢氧化钠溶液,过滤,用蒸馏水洗涤沉淀后用稀盐酸溶解沉淀 | |
| C. | 除去K2CO3固体中少量NaHCO3:置于坩埚中加热 | |
| D. | 用盐酸除去AgCl中少量的Ag2CO3 |
11.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入硝酸银,产生白色沉淀,再加稀硝酸,沉淀不溶解,则溶液中一定有Cl- | |
| D. | 加入KSCN,溶液变血红色,则溶液中一定有Fe2+ |
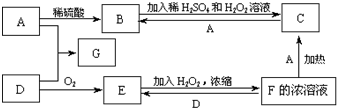 中学化学中几种常见物质的转化关系如图(有部分产物未画出).A是一种金属单质,D是一种非金属固体单质.
中学化学中几种常见物质的转化关系如图(有部分产物未画出).A是一种金属单质,D是一种非金属固体单质.