题目内容
【题目】若NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.标准状况下,22.4L SO3含NA个分子
B.含0.4mol HCl的浓盐酸与足量二氧化锰反应转移电子数为0.2NA
C.32gCu与足量硫完全反应,转移的电子数为0.5NA
D.在200mL 5mol·L-1 AlCl3溶液中,Al3+数目为NA,等于Cl-数目的1/3
【答案】C
【解析】
本题考查物质的量计算,A.标准状况下的物质状态;B.反应的消耗量;C.反应前后变价情况;D.水解的考查。
A.标准状况下,SO3是固体,不能使用![]() ,A错误;
,A错误;
B.浓盐酸与足量二氧化锰反应过程中,浓盐酸不仅会挥发一部分而且在反应一段时间后浓盐酸会变成稀盐酸,就不会和二氧化锰反应,因此0.4mol HCl的HCl并不能全部参加反应,B错误;
C.Cu与足量硫完全反应,不仅Cu完全参加反应,而且会生成+1价态的亚铜(Cu2S),一个Cu转移一个电子,所以消耗铜和转移电子的个数比或物质的量比为1:1,m(Cu)=32g,那么![]() ,所以转移电子数为0.5NA,C正确;
,所以转移电子数为0.5NA,C正确;
D.由于Al3+会发生水解,在水溶液中Al3+存在的会比NA少,所以![]() 小于
小于![]() ;。
;。

 阅读快车系列答案
阅读快车系列答案【题目】几种物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净CuCl2溶液,宜加入___________调至溶液pH=4,使Fe3+转化为Fe(OH) 3沉淀,此时溶液中的c(Fe3+)=_____________。
(2)过滤后,将所得滤液经过________,________操作,可得到CuCl2·2H2O晶体。
(3)由CuCl2·2H2O晶体得到纯的无水CuCl2,需要进行的操作是________________。
(4)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.800 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。过滤后,滤液用0.1000 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液40.00 mL。(已知:I2+2S2O32-=S4O32-+2I-)。
①可选用________作滴定指示剂,滴定终点的现象是__________________________。
②CuCl2溶液与KI反应的离子方程式为________________________________。
③该试样中CuCl2·2H2O的质量百分数为________。
【题目】从镍矿石尾矿中提取NiSO4是解决我国镍资源匮乏的一条重要途径,已知该过程如下:
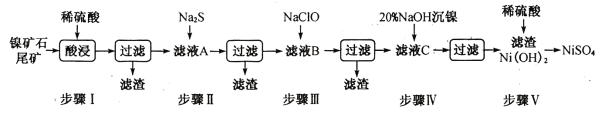
表1:各物质的Ksp数据如下表:
物质 | MnS | NiS | PbS | CuS | Ni(OH)2 |
Ksp | 2.5×10-13 | 1.1×10-21 | 8.0×10-28 | 6.3×10-36 | 2.0×10-15 |
表2:滤液A中各金属离子的含量如下表:
成分 | Ni2+ | Fe3+ | Fe2+ | Mn2+ | Cu2+ | Pb2+ | …… |
含量/g·L-1 | 3.80 | 4.80 | x | 0. 20 | 0.15 | <0.001 | …… |
根据以上信息,回答下列问题:
(1)步骤I酸浸之前需将矿石粉碎,目的是_______________。
(2)
(3)常温下进行步骤Ⅲ的目的是为了除去铁和锰元素,已知除铁元素的离子反应如下:2Fe2++ ClO - +5H2O=2Fe( OH)3↓+Cl- +4H+,此时Mn2+的氧化产物为MnO2,写出除锰元素的离子方程式_____________。
(4)所得Ni(OH)2是制造镍镉电池的重要原料,镍镉电池工作原理如下:Cd+2NiO(OH) +2H2O![]() Cd(OH)2+2Ni(OH)2,则随着放电的进行,正极区pH______(填“增大”、“减小”或“不变”);充电时阴极电极反应式为______________________。
Cd(OH)2+2Ni(OH)2,则随着放电的进行,正极区pH______(填“增大”、“减小”或“不变”);充电时阴极电极反应式为______________________。