题目内容
【题目】向二元弱酸H2Y溶液中滴加KOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示。下列有关说法正确的是
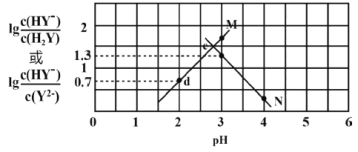
A.曲线N表示pH与![]() 的变化关系
的变化关系
B.交点e的溶液中:c(H2Y)=c(Y2-)>c(HY-)>c(H+)>c(OH-)
C.d点溶液中:c(H+)-c(OH-)=c(Y2-)+c(HY-)-c(K+)
D.Ka2(H2Y)=10-4.3
【答案】D
【解析】
H2Y溶液中滴加KOH溶液,随着pH的不断增大,先发生H2Y+OH-=HY-+H2O,后发生HY-+OH-=Y2-+H2O。
A. 按反应的先后次序,可确定曲线N表示pH与![]() 的变化关系,A不正确;
的变化关系,A不正确;
B. 交点e的溶液中,![]() =
=![]() ,由此得出c(H2Y)=c(Y2-),由反应H2Y+OH-=HY-+H2O、HY-+OH-=Y2-+H2O的顺序,可确定c(HY-)>c(H2Y)=c(Y2-)>c(H+)>c(OH-),B不正确;
,由此得出c(H2Y)=c(Y2-),由反应H2Y+OH-=HY-+H2O、HY-+OH-=Y2-+H2O的顺序,可确定c(HY-)>c(H2Y)=c(Y2-)>c(H+)>c(OH-),B不正确;
C. 依电荷守恒,d点溶液中:c(H+)-c(OH-)=2c(Y2-)+c(HY-)-c(K+),C不正确;
D. 根据图像当pH=3时![]() =1.3,H2Y的第二步电离方程式为HY-
=1.3,H2Y的第二步电离方程式为HY-![]() H++Y2-,Ka2(H2Y)=
H++Y2-,Ka2(H2Y)=![]() =
= ![]() =10-4.3,D正确;
=10-4.3,D正确;
故选D。

【题目】已知反应2A(g)+2B(g)![]() C(g)+2D(g),在容器均为2L的甲,乙,丙三个恒温(反应温度分别为300℃,T℃,300℃)容器中分别加入物质的量之比为1:1的A和B,测得各容器中n(B)随反应时间t的变化情况如下表所示:
C(g)+2D(g),在容器均为2L的甲,乙,丙三个恒温(反应温度分别为300℃,T℃,300℃)容器中分别加入物质的量之比为1:1的A和B,测得各容器中n(B)随反应时间t的变化情况如下表所示:
0 | 40 | 80 | 120 | 160 | |
甲 | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
乙 | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
丙 | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
根据表中数据,下列说法正确的是
A.乙容器中的反应温度T<300
B.丙容器中,0-40min内用A的浓度变化表示的平均反应速率为为0.05mol/(L·min)
C.若起始时向甲容器中加入0.2、0.2、0.4和1.2,则反应将向正反应方向进行
D.在0-40min内,提高乙容器中的A的转化率的有效途径是使用高效催化剂