题目内容
【题目】某同学实验探究氨气的还原性并进行系列实验。
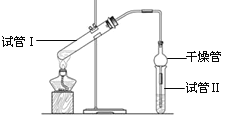
(1)将光亮的紫红色铜丝绕几圈后,在酒精灯火焰上加热,等铜丝变黑后,趁热将铜丝插入疏松的氯化铵晶体里,即刻发现有白色烟雾生成,拿出铜丝后,铜丝又转变为光亮的紫红色。在焊接铜器时用氯化铵除去铜器表面的氧化铜即利用了该原理,请完成该反应:
![]()
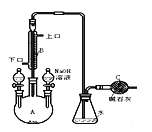
(2)利用下列装置,进行与金属氧化物MxOy反应生成M、H2、H2O,通过测量生成水的质量来测定M的相对原子质量。a中试剂是浓氨水。
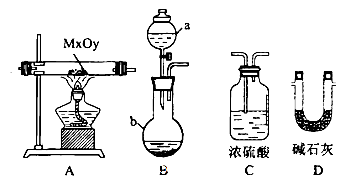
①仪器a的名称为__________,仪器b中装人的试剂可以是____________.
②按气流方向正确的装置连接顺序为(填序号,装置可重复使用):___________。
③实验结束时,应首先__________(填序号)。
I.熄灭A装置的酒精灯
II.停止从a中滴加液体
④若实验中准确称取金属氧化物的质量为mg,完全反应后,测得生成水的质量为ng,则M的相对原子质量为__________ (用含X、y、m、n的式子表示)。
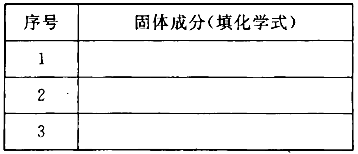
(3)若金属氧化物MxOy为Fe2O3,将反应后固体溶于稀硫酸,然后滴加KSCN溶液没发生明显变化。推测该固体成分可能是(将化学式填人下表,你认为有几种可能填几种)。
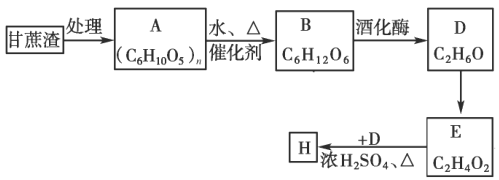
【答案】(1)4CuO + 2NH4Cl=3Cu +CuCl2+ 4H2O(2)①分液漏斗,,氢氧化钠或碱石灰;②BDADC;③实验结束时,应首先停止从a中滴加液体,没有必要制备多余的氨气;④(18m-16n)y/nx (3)铁铁或者是铁和三氧化二铁
【解析】
试题分析:(1)根据化合价升降法进行配平,可得4CuO + 2NH4Cl=3Cu +CuCl2+ 4H2O
(2)①根据仪器的特征,仪器a的名称为分液漏斗,仪器b中装入的试剂可以是氢氧化钠或碱石灰,通过吸收水有利于制备出氨气。
②从发生装置中出来的氨气带有水份,必须要进行干燥,所以B接D,D接A,吸收反应生成的水要用D装置,最后空气中的水不能进入到D中,还要用到C,因此,按气流方向正确的装置连接顺序为BDADC。③实验结束时,应首先停止从a中滴加液体,没有必要制备多余的氨气。
④根据氧元素守恒,MxOy—— yH2O,已知金属氧化物的质量为mg,生成水的质量为ng,则m:n=(xM+16y):18y,求得M的相对原子质量为(18m-16n)y/nx。
(3)若金属氧化物MxOy为Fe2O3,将反应后固体溶于稀硫酸,然后滴加KSCN溶液没发生明显变化。说明溶液中没有三价铁离子,因为Fe+2Fe3+= 3Fe2+,所以反应后的固体成分可能全是铁,或者是铁和三氧化二铁。