题目内容
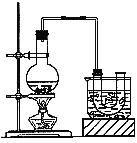
【题目】制备溴苯的实验装置如右图所示,请回答下列问题:
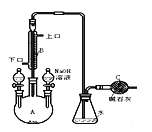
(1)反应开始前已向仪器A中加入的固体药品是铁粉,则装在左侧分液漏斗中的液体药品是 。
(2)写出实验室制溴苯的化学方程式 。
(3)该反应装置中冷凝管B有上、下两个口,冷却水应从 口进入(填“上”或“下”)。
(4)右侧分液漏斗中的物质在 加入A中(填“反应前”、“反应中”或“反应后”),用离子方程式表示其作用是 。
(5)C中碱石灰的作用是 。
(6)该过程可以如下表述:3Br2+2Fe=2FeBr3 ; Br2+FeBr3=FeBr4-+Br+ (不稳定) ;
![]() +Br+→[
+Br+→[![]() ] ; [
] ; [![]() ]+FeBr4-→
]+FeBr4-→![]() +HBr+FeBr3 。
+HBr+FeBr3 。
由上述反应可推知:![]() +Br2 →
+Br2 → ![]() +HBr 中的催化剂为 。(填字母)
+HBr 中的催化剂为 。(填字母)
A. Br2 B.FeBr3 C.Br+ D.FeBr4-
【答案】(1)苯、液溴 (2) (3) 下口(4)反应后 Br2+2OH-=Br-+BrO-+ H2O
(3) 下口(4)反应后 Br2+2OH-=Br-+BrO-+ H2O
(5)吸收多余HBr,防止污染空气 (6)BD
【解析】
试题分析:(1)苯与液溴在铁作催化剂的条件下发生取代反应生成溴苯;装在左侧分液漏斗中的液体药品是苯、液溴。
(2)实验室制溴苯的化学方程式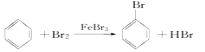 。
。
(3)冷凝管B有上、下两个口,冷却水应从下口进入。
(4)氢氧化钠的作用是除去溴苯中的溴单质,在反应后加入A中,离子方程式Br2+2OH-=Br-+BrO-+ H2O。
(5)C中碱石灰的作用是吸收多余HBr,防止污染空气。
(6)由上述反应可推知:![]() +Br2 →
+Br2 → ![]() +HBr 中的催化剂为FeBr3、FeBr4-。
+HBr 中的催化剂为FeBr3、FeBr4-。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目