题目内容
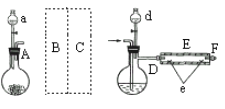
【题目】现有一定量含有Na2O杂质的Na2O2试样,用如图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6mol·L-1盐酸、6mol·L-1硫酸和蒸馏水)
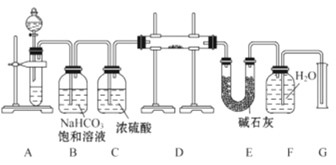
回答下列问题:
(1)装置A中液体试剂选用________
(2)装置B的作用是_________________,装置C的作用是_____________,装置E中碱石灰的作用是______________________________________________。
(3)装置D中发生反应的化学方程式是_________________________。
(4)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为_____________________________________。
【答案】6mol·L-1盐酸 除去气体中的HCl 干燥气体 吸收装置D中反应剩余的CO2 2Na2O2+2CO2=2Na2CO3+O2、Na2O+CO2=Na2CO3 78%
【解析】
实验的目的是测定Na2O2试样的纯度,其中杂质为Na2O;根据所给装置,本实验中是要通过测定二氧化碳二氧化碳与Na2O2反应生成的氧气的量来确定样品中过氧化钠的量,所以首先在装置A中利用碳酸钙和盐酸反应生成二氧化碳,用饱和碳酸氢钠溶液除去CO2中混有的HCl气体,之后用浓硫酸进行干燥,然后在装置D中CO2和Na2O2反应生成氧气,用碱石灰吸收未反应的CO2,氧气不易溶于水,可以用排水法测定生成的氧气的体积。
(1)装置A的目的是制取二氧化碳,一般用盐酸和碳酸钙反应制取二氧化碳,所以装置A中液体试剂为盐酸;
(2)装置B可以除去CO2中混有的HCl气体;浓硫酸具有吸水性,所以装置C干燥气体;装置E中的碱石灰吸收未反应的CO2,避免对氧气体积的测定产生影响;
(3)装置D中为CO2和Na2O2、Na2O的反应,化学方程式为2Na2O2+2CO2=2Na2CO3+O2、Na2O+CO2=Na2CO3;
(4)生成的氧气体积为224mL,物质的量为![]() =0.01mol,根据反应方程式可知样品中Na2O2的物质的量为0.02mol,所以样品的纯度为
=0.01mol,根据反应方程式可知样品中Na2O2的物质的量为0.02mol,所以样品的纯度为![]() =78%。
=78%。

 名校课堂系列答案
名校课堂系列答案