题目内容
【题目】Ti、Fe、Cu、Ni为过渡金属元素,在工业生产中有重要的应用.
(1)①常温下Fe(CO)5呈液态,熔点为-20.5℃,沸点为103℃.据此可以判断其晶体为_________晶体,Fe(CO)5中铁的化合价为0,则该物质中含有的化学键类型有______(填字母).
A 离子键 B 极性共价键 C 非极性共价键 D 配位键
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为________,配体H2O中O原子的杂化方式为________.
③NiO、FeO的晶体结构类型均与氧化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO_______FeO(填“<”或“>”).
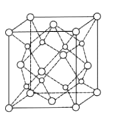
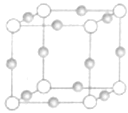
(2)Cu、N两元素形成某种化合物的晶胞结构如图(灰色球表示Cu原子),已知紧邻的白球与灰球之间的距离为acm,该晶胞的密度为________gcm-3.
【答案】分子晶体 BD 6 sp3杂化 >; ![]()
【解析】
(1)①Fe(CO)5熔沸点比较低,符合分子晶体性质;Fe与CO之间形成配位键,CO中存在极性键;
②配离子[Fe(NO)(H2O)5]2+中Fe2+是中心离子,NO、H2O是配体;H2O中O原子形成2个O-H键,含有2对孤对电子,杂化轨道数目为4;
③离子电荷相同,离子半径越小,晶格能越大,离子晶体的熔沸点越高;
(2)紧邻的白球与灰球之间的距离为acm,则晶胞棱长为2a cm,根据均摊法计算晶胞中Cu、N原子数目,表示出晶胞质量,再根据ρ=![]() 计算晶胞密度。
计算晶胞密度。
(1)①常温下Fe(CO)5呈液态,熔点为-20.5℃,沸点为103℃,符合分子晶体性质,应使用分子晶体;Fe与CO之间形成配位键,CO中存在极性键;
②配离子[Fe(NO)(H2O)5]2+中Fe2+是中心离子,NO、H2O是配体,Fe2+的配位数为6;H2O中O原子形成2个O-H键,含有2对孤对电子,杂化轨道数目为4,O原子采取sp3杂化;
③NiO、FeO的晶体结构类型均与氧化钠的相同,均属于离子晶体,离子电荷相等,而离子半径Ni2+<Fe2+,故NiO的晶格能大于FeO的,则熔点NiO>FeO;
(2)紧邻的白球与灰球之间的距离为a cm,则晶胞棱长为2a cm,晶胞中Cu原子数目为12×![]() =3、N原子数目=8×
=3、N原子数目=8×![]() =1,则晶胞质量为
=1,则晶胞质量为![]() g,则晶胞密度为
g,则晶胞密度为![]() g÷(2acm)3=
g÷(2acm)3=![]() gcm-3。
gcm-3。

【题目】相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g) + 3H2(g) ![]() 2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量a kJ |
② | 2 | 3 | 0 | 放出热量b kJ |
③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是
A. 放出热量关系:a < b <92.4
B. 三个容器内反应的平衡常数:③>①>②
C. 达平衡时氨气的体积分数:①>③
D. N2的转化率:②>①>③