题目内容
【题目】纯碱(Na2CO3)在生产生活中具有广泛的用途.如图1是实验室模拟制碱原理制取Na2CO3的流程图.
完成下列填空:
已知:粗盐中含有Ca2+、Mg2+、SO42﹣等杂质离子.
(1)精制除杂的步骤顺序是____→___→____→____→____ (填字母编号).
a 粗盐溶解 b 加入盐酸调pH c 加入Ba(OH)2溶液 d 加入Na2CO3溶液 e 过滤
(2)向饱和食盐水中先通入NH3,后通入CO2,理由是______.在滤液a中通入NH3和加入精盐的目的是______.
(3)请在图1流程图中添加两条物料循环的路线.____

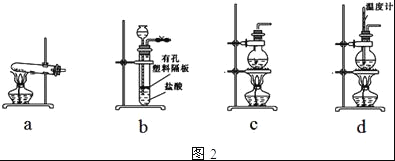
(4)图2装置中常用于实验室制备CO2的是__(填字母编号);用c装置制备NH3,烧瓶内可加入的试剂是___(填试剂名称).
(5)一种天然碱晶体成分是aNa2CO3bNa2SO4cH2O,利用下列提供的试剂,设计测定Na2CO3质量分数的实验方案.请把实验方案补充完整:
供选择的试剂:稀H2SO4、BaCl2溶液、稀氨水、碱石灰、Ba(OH)2溶液
①______.
②______.
③______.
④计算天然碱晶体中含Na2CO3的质量分数.
【答案】a c d e b NH3易溶于水,有利于吸收溶解度不大的CO2 NH3溶于水能将HCO3﹣转化为CO32﹣,并增大加入NH4+浓度;加入精盐增大Cl﹣浓度,有利于NH4Cl结晶析出 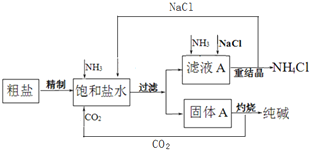 b 浓氨水 称取一定质量的天然碱晶体 加入足量稀硫酸并微热、产生的气体通过足量Ba(OH)2溶液 过滤、洗涤、干燥、称量、恒重沉淀
b 浓氨水 称取一定质量的天然碱晶体 加入足量稀硫酸并微热、产生的气体通过足量Ba(OH)2溶液 过滤、洗涤、干燥、称量、恒重沉淀
【解析】
(1)根据SO42﹣、Ca 2+、Mg2+等易转化为沉淀而被除去,以及根据不能产生新杂质的要求排序,前面加入的过量溶液应用后加入的溶液除去,最后加入适量的溶液;
(2)NH3易溶于水,有利于吸收溶解度不大的CO2;根据溶解平衡,增加反应物的浓度有利于晶体析出;
(3)侯氏制碱法主要操作是在氨化饱和的NaCl溶液里通CO2,因此后续操作中得到的CO2和NaCl可循环利用;
(4)实验室制取二氧化碳的反应原理和条件;根据在浓氨水中加碱或生石灰,因为氨水中存在下列平衡:NH3+H2ONH3H2ONH4++OH﹣加入碱或生石灰产生氢氧根离子平衡左移,同时放出大量的热促进氨水的挥发,制得氨气;
(5)根据实验的原理:先称取一定量的天然碱晶体并溶解得到水溶液,将碳酸根全部转换成二氧化碳,利用二氧化碳和澄清石灰水产生沉淀,通过沉淀的质量求出二氧化碳的物质的量、Na2CO3的物质的量和质量,最终求出Na2CO3的质量分数。
(1)SO42﹣、Ca2+、Mg2+等分别与Ba(OH)2溶液、Na2CO3溶液、Ba(OH)2溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的Ba(OH)2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加Ba(OH)2溶液再加Na2CO3溶液,过滤,最后加入盐酸,故答案为:a→c→d→e→b;
(2)NH3易溶于水,有利于吸收溶解度不大的CO2,所以向饱和食盐水中先通入NH3,后通入CO2;通入NH3可通过与HCO3﹣的反应,增加NH4+浓度,并利用精盐增大Cl﹣浓度,根据溶解平衡的移动,有利于NH4Cl结晶析出;
(3)煅烧炉里生成的CO2可循环利用,滤液a析出晶体氯化铵后得到的NaCl溶液可循环利用,则 ;
;
(4)实验室制取二氧化碳常选用石灰石和稀盐酸或大理石和稀盐酸反应制取,采用固体+液体![]() 气体;浓氨水中加碱或生石灰,因为氨水中存在下列平衡:NH3+H2ONH3H2ONH4++OH﹣,加入碱平衡左移,同时放出大量的热促进氨水的挥发,制得氨气;
气体;浓氨水中加碱或生石灰,因为氨水中存在下列平衡:NH3+H2ONH3H2ONH4++OH﹣,加入碱平衡左移,同时放出大量的热促进氨水的挥发,制得氨气;
(5)实验的原理:先称取样品质量并溶解,将碳酸根全部转换成二氧化碳,利用二氧化碳和澄清石灰水产生沉淀,通过沉淀的质量求出二氧化碳的物质的量、Na2CO3的物质的量和质量,最终求出Na2CO3的质量分数,所以将天然碱晶体样品,溶于适量蒸馏水中,加入足量稀硫酸并微热,产生的气体通过足量的澄清石灰水,然后过滤、洗涤、干燥、称量沉淀即可。

【题目】下表列出了元素周期表中前20号元素中某些元素性质的一些数据:
性质元素 | 原子半径( | 最高价态 | 最低价态 |
① | 1.02 |
|
|
② | 2.27 |
| — |
③ | 0.74 | — |
|
④ | 1.43 |
| — |
⑤ | 0.77 |
|
|
⑥ | 1.10 |
|
|
⑦ | 0.99 |
|
|
⑧ | 1.86 |
| — |
⑨ | 0.75 |
|
|
⑩ | 1.17 |
|
|
试回答下列问题。
(1)以上10种元素中,第一电离能最小的是______(填序号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质有______(填分子式,两种即可)。元素⑨和⑩形成的化合物的化学式为______;元素①的原子价电子排布式是______。
(3)①、⑥、⑦、⑩四种元素的简单氢化物的稳定性由强到弱的顺序是______(填化学式)。
(4)③和⑨两元素相比,非金属性较弱的是______(填名称),可以验证该结论的是______(填序号)。
A.气态氢化物的挥发性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.最简单氢化物的稳定性
F.两单质在自然界中的存在形式
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl22H2O的流程如下:
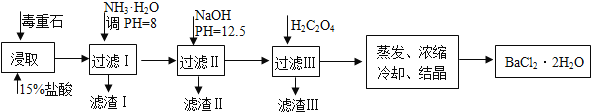
完成下列填空:
(1)毒重石用盐酸浸取前需充分研磨,目的是____________________。实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的____________________________。
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)加入NH3H2O调节pH=8可除去_______(填离子符号),滤渣Ⅱ 中含__________(填化学式)。加入H2C2O4时应避免过量,原因是_________________________。
已知:Ksp(BaC2O4)=1.6×10﹣7,Ksp(CaC2O4)=2.3×10﹣9
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |