题目内容
13.X、Y、Z、W、R五种短周期元素原子序数依次增大,X是周期表中原子半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,W单质是人类将太阳能转变为电能的常用材料.下列说法正确的是( )| A. | 热稳定性:X2R>X2Y | |
| B. | WY2能与碱反应,但不能与任何酸反应 | |
| C. | Z位于第三周期第ⅢA族,Z与Y形成的化合物是一种比较好的耐火材料 | |
| D. | 使甲基橙变红色的溶液中:K+、R2-、ZY2-、WY32- 一定能大量共存 |
分析 X是周期表中原子半径最小的元素,应为H元素,Y原子最外层电子数是次外层电子数的3倍,应为O元素,R与Y处于同一族,R应为S元素,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,Z应为Al元素,W单质是人类将太阳能转变为电能的常用材料,则W为Si元素;结合对应单质、化合物的性质以及元素周期律知识解答该题.
解答 解:X是周期表中原子半径最小的元素,应为H元素,Y原子最外层电子数是次外层电子数的3倍,应为O元素,R与Y处于同一族,R应为S元素,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,Z应为Al元素,W单质是人类将太阳能转变为电能的常用材料,则W为Si元素;
A.元素的非金属性越强,其氢化物越稳定,则热稳定性:H2O>H2S,即热稳定性:X2R<X2Y,故A错误;
B.SiO2能与碱反应,也能与HF反应,故B错误;
C.Al位于第三周期第ⅢA族,Al与O形成的化合物氧化铝的熔点很高,是一种比较好的耐火材料,故C正确;
D.使甲基橙变红色的溶液中,说明含有氢离子,则S2-、AlO2-、CO32- 不能大量共存,故D错误.
故选C.
点评 本题考查原子结构与元素周期律知识,为高考常见题型,侧重于学生的分析能力的考查,难度中等,注意把握原子结构特征和对应单质、化合物的性质,学习中注意相关基础知识的积累.

练习册系列答案
相关题目
4.如表是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B的质量数的2.5倍,B元素的原子核内质子数等于中子数.
(1)写出A、B、C三种元素符号:P、O、Cl
(2)B元素位于周期表中第二周期第ⅥA族
(3)C的气态氢化物水溶液显酸性(填“酸”或“碱”)
| B | ||
| A | C |
(2)B元素位于周期表中第二周期第ⅥA族
(3)C的气态氢化物水溶液显酸性(填“酸”或“碱”)
8.溶质质量分数分别为c和5c的硫酸溶液,按等质量混合均匀后,混合溶液中硫酸的质量分数为 ( )
| A. | 3c | B. | 6c | C. | >3c | D. | <3c |
2.化学与生活、社会密切相关,下列说法不正确的是( )
| A. | 碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜锡合金 | |
| B. | 氨很容易液化,液氨气化吸收大量的热,所以液氨常用作致冷剂 | |
| C. | Al2O3用作耐火材料、Al(OH)3用作阻燃剂 | |
| D. | SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等 |
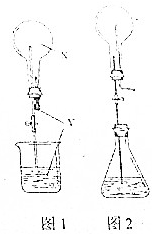 关于喷泉实验,回答下列问题:
关于喷泉实验,回答下列问题:
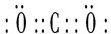 .
.