题目内容
19.如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是( )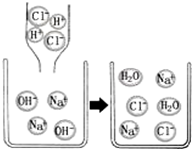
| A. | 反应前后所有元素种类不变 | |
| B. | 恰好反应后溶液的pH大于7 | |
| C. | 反应前的溶液可导电,反应后的溶液不导电 | |
| D. | 中和反应的实质是Na+和Cl-反应生成NaCl |
分析 A.化学反应是最小微粒是原子;
B.反应后的溶液中只有氯离子、钠离子、水分子,所以pH等于7;
C.反应后的溶液中存在带正电的钠离子和带负电的氯离子;
D.中和反应的实质是酸电离的氢离子和碱电离的氢氧根离子相互作用生成水分子的过程.
解答 解:A.化学反应是最小微粒是原子,元素种类不变,故A正确;
B.根据反应后的容器中的离子可以看出,反应后的溶液中没有氢氧根离子,只有氯离子、钠离子、水分子,所以pH等于7,故B错误;
C.溶液导电是靠溶液中带电的离子导电的,反应后的溶液中存在带正电的钠离子和带负电的氯离子,所以反应后的溶液能导电,故C错误;
D.中和反应的实质是H++OH-═H20,故D错误.
故选A.
点评 本题主要从微观图示的角度对中和反应和相关的知识进行了考查,涉及了了溶液的导电性、酸碱性和PH值的关系,难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
9.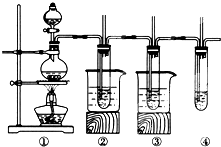 在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去).图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液.
在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去).图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液.
(1)③试管中制取次氯酸钠的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O
(2)实验中可观察到④试管中溶液的颜色发生如下变化,填写表格.
(3)此实验有一个明显的不足之处,应如何改进?④后增加一个盛有氢氧化钠溶液的烧杯用于吸收多余的氯气.
 在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去).图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液.
在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去).图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液.(1)③试管中制取次氯酸钠的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O
(2)实验中可观察到④试管中溶液的颜色发生如下变化,填写表格.
| 实验现象 | 原因 |
| 溶液最初从紫色变为红色 | 氯气与水反应生成的HCl使石蕊试液变红 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成HClO具有漂白性 |
| 最后溶液从无色逐渐变为浅黄绿色 | 过量氯气溶解于水中 |
10.具有下列价电子数的原子,最难形成离子的是( )
| A. | L层6个 | B. | L层4个 | C. | M层2个 | D. | M层7个 |
7.心脏起搏器一般是给心跳缓慢的病人使用.某种类型的心脏起搏器工作时发生下列反应:4Li+2SOCl2═4LiCl+S+SO2下列有关判断正确的是( )
| A. | 还原剂只有锂 | |
| B. | 标准状况下生成1.12LSO2时,反应转移电子为0.1mol | |
| C. | 氧化产物包括LiCl和SO2 | |
| D. | SOCl2中既有离子键,也有共价键 |
14.下列关于电解质的叙述正确的是( )
| A. | 强酸、强碱及大部分盐类属于强电解质,弱酸、弱碱属于弱电解质 | |
| B. | 所有的离子化合物都是强电解质,所有的共价化合物都是弱电解质 | |
| C. | 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 | |
| D. | CO2的水溶液能导电,所以CO2是电解质 |
8.在呼吸面具和潜水艇中可以用过氧化钠作为供氧剂.某化学探究学习小组选用适当的化学试剂和实验用品,用下图中实验装置,进行实验来证明过氧化钠可作供氧剂.其中,
A是实验室制取CO2的装置,D中装有过氧化钠固体.
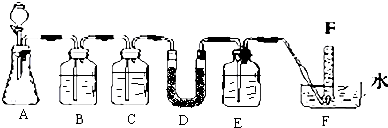
(1)写出A装置中发生反应的离子方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)填写表中空格:
(3)若无C装置,对实现该实验目的是否有影响否(填“是”或“否”),原因(化学方程式表示)2Na2O2+2H2O=4NaOH+O2;
(4)试管F中收集满气体并从水中取出后,下一步实验操作为:立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.
(5)写出D中发生反应的化学方程式,并用双线桥标注出电子转移情况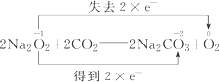 .
.
A是实验室制取CO2的装置,D中装有过氧化钠固体.

(1)写出A装置中发生反应的离子方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | 除去CO2中的水蒸气 | |
| E |
(4)试管F中收集满气体并从水中取出后,下一步实验操作为:立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.
(5)写出D中发生反应的化学方程式,并用双线桥标注出电子转移情况
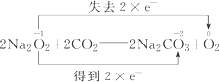 .
.  .
.