题目内容
4.(1)有一只烧瓶,在标准状况下,当充满空气时,重152.34g,充满O2时重 152.37g,充满CO2时重152.49g.(2)在一定条件下,有aLO2和O3的混合气,当其中的O3全部转化为O2时,体积变为1.2aL,原混合气中O2的质量分数为50%.
分析 (1)同温同压下,相同容积时气体的物质的量相同.令气体的物质的量为n,容器质量为m,根据容器充满空气与氧气的质量,列方程计算n、m的值,再根据m=nM计算二氧化碳的质量,进而计算充满二氧化碳时总质量;
(2)发生反应:2O3=3O2 ,利用差量法计算混合气体中O3的体积,相同条件下气体体积之比等于物质的量之比,再根据m=nM计算质量之比,进而计算氧气质量分数.
解答 解:(1)相同条件下,气体体积之比等于物质的量之比,令空气、O2、CO2的物质的量分别为n mol、容器质量为m,则:
m+n×29g/mol=152.34g,
m+n×32g/mol=152.37g,
解得,n=0.01mol,m=152.05g,
故充满CO2时重:152.05g+0.01mol×44g/mol=152.49g,
故答案为:152.49.
(2)设混合气体中O3体积为V,则:
2O3=3O2 体积增大
2 1
V 1.2aL=aL=0.2aL
所以V=0.4aL
故O2的体积为aL-0.4aL=0.6aL
则O2、O3的物质的量之比为0.6aL:0.4aL=3:2,二者质量之比为3mol×32g/mol:2mol×48g/mol=1:1,
故混合气体中O2的质量分数为$\frac{1}{1+1}$×1005=50%,
故答案为:50%.
点评 本题考查物质的量有关计算、阿伏伽德罗定律等,难度不大,旨在考查学生等于基础知识的掌握.

练习册系列答案
相关题目
12.工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3气体,已知该反应为放热反应.现将2mol SO2、1mol O2充入一密闭容器充分反应后,放出热量98.3kJ,此时测得SO2的转化率为50%,则下列热化学方程式正确的是( )
| A. | 2SO2(g)+O2(g)?2SO3(g)△H=-196.6 kJ•mol-1 | |
| B. | 2SO2(g)+O2(g)?2SO3(g)△H=-98.3 kJ•mol-1 | |
| C. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=+98.3 kJ•mol-1 | |
| D. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-196.6 kJ•mol-1 |
19.如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是( )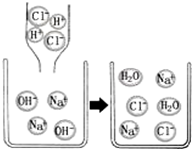

| A. | 反应前后所有元素种类不变 | |
| B. | 恰好反应后溶液的pH大于7 | |
| C. | 反应前的溶液可导电,反应后的溶液不导电 | |
| D. | 中和反应的实质是Na+和Cl-反应生成NaCl |
9.根据某种共性,可将SO2、CO2归为同类氧化物.下列物质中也属于这类氧化物的是( )
| A. | CaCO3 | B. | SO3 | C. | KMnO4 | D. | Na2O |
16.光照下或暴露在空气中,不发生化学变化的一项是( )
| A. | 金属钠 | B. | Na2O | C. | 新制的氯水 | D. | NaCl |