题目内容
11.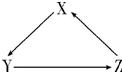 X、Y、Z为中学化学常见物质,其转化关系如下图所示(“→”表示一步转化).下列组合不正确的是( )
X、Y、Z为中学化学常见物质,其转化关系如下图所示(“→”表示一步转化).下列组合不正确的是( )| 选项 | X | Y | Z |
| A | Al | Al(OH)3 | Al2O3 |
| B | Na | Na2O2 | NaOH |
| C | H2SO3 | SO2 | H2SO4 |
| D | HCl | Cl2 | HClO |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Al不能一步转化为氢氧化铝;
B.钠在空气中燃烧生成过氧化钠,过氧化钠与水反应生成氢氧化钠,氢氧化钠不能一步转化为金属钠;
C.亚硫酸分解得到二氧化硫,二氧化硫与氢氧化钠反应得到亚硫酸钠,亚硫酸钠和盐酸反应得到亚硫酸;
D.次氯酸与氯化物反应可以生成氯气,氯气与水反应得到HCl,次氯酸分解可以得到HCl.
解答 解:A.Al不能一步转化为氢氧化铝,不符合转化关系,故A选;
B.钠在空气中燃烧生成过氧化钠,过氧化钠与水反应生成氢氧化钠,氢氧化钠不能一步转化为金属钠,不符合转化关系,故B选;
C.亚硫酸分解得到二氧化硫,二氧化硫与氢氧化钠反应得到亚硫酸钠,亚硫酸钠和盐酸反应得到亚硫酸,符合转化关系,故C不选;
D.盐酸与高锰酸钾等强氧化剂发生氧化还原反应可以生成氯气,而氯气与水反应可以得到HClO,HClO分解得到盐酸,符合转化关系,故D不选.
故选AB.
点评 本题考查元素化合物性质,利用验证法进行解答,需要学生熟练掌握知识,难度中等.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
2.下列反应不属于氧化还原反应的是( )
| A. | 碳酸氢钠受热分解 | B. | 铝和三氧化二铁高温下反应 | ||
| C. | 过氧化钠与水反应 | D. | 铜和浓硫酸反应 |
19.烷烃①3,3-二甲基戊烷;②正庚烷;③2-甲基己烷;④正丁烷.沸点由高到低的顺序是( )
| A. | ③>①>②>④ | B. | ①>②>③>④ | C. | ②>③>①>④ | D. | ②>①>③>④ |
6.下列有关说法不正确的是( )
| A. | 胶体的丁达尔效应与微粒直径大小有关 | |
| B. | 电解质溶液的导电能力与溶液中离子浓度及离子所带电荷多少有关 | |
| C. | CaO的水溶液能够导电,因此Ca0是电解质 | |
| D. | 向饱和氯化钠溶液中加人一小块钠,溶液中有固体析出 |
3.对于反应:TiCl4+4Na═4NaCl+Ti,下列说法正确的是( )
| A. | 该反应说明钠是强还原剂,可用于冶炼金属 | |
| B. | 该反应条件是TiCl4在熔融状态或水溶液中 | |
| C. | Ti是氧化产物 | |
| D. | TiCl4是还原剂 |
20.下列物质中能抑制水的电离且使溶液呈现出酸性的是( )
| A. | Na2CO3 | B. | NaOH | C. | K2SO4 | D. | H2SO4 |
1.某温度下,在体积固定不变的密闭容器中进行如下可逆反应:X(g)+Y(g)?Z(g)+W(s)△H>0,下列叙述不正确的是( )
| A. | 当容器中气体压强不变时,反应达到平衡 | |
| B. | 升高温度,平衡正向移动 | |
| C. | 加入少量W,逆反应速率增大 | |
| D. | 当气体密度不变时,说明反应达到平衡 |
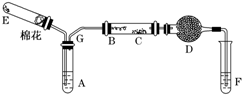 如图所示为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中,A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水硫酸铜粉末,D为碱石灰,F为新制的Cu(OH)2悬浊液.(提示:乙醇催化氧化产物与新制Cu(OH)2悬浊液共热有砖红色沉淀生成)
如图所示为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中,A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水硫酸铜粉末,D为碱石灰,F为新制的Cu(OH)2悬浊液.(提示:乙醇催化氧化产物与新制Cu(OH)2悬浊液共热有砖红色沉淀生成)