题目内容
下列是工业上制取合成氨原料气氢气的一步重要反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0 ,该反应达到平衡后,为提高CO的转化率,下列措施中正确的是
| A.增大压强 | B.降低温度 | C.增大CO的浓度 | D.更换催化剂 |
B
解析试题分析:提高CO的转化率可以让平衡正向进行即可。A、增加压强,该平衡会不会发生移动,故A错误;B、降低温度,化学平衡向着放热方向即正向进行,故B正确;C、增大CO的浓度,化学平衡向着正方向进行,但是一氧化碳的转化率降低,故C错误;D、催化剂不会引起化学平衡的移动,故D错误。
考点:化学平衡的影响因素

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
下列事实中,能用勒沙特列原理来解释的是
| A.由H2(g)、I2(g)、HI(g)组成的混合气体平衡体系加压后颜色加深 |
| B.久置的氯水变成了稀盐酸 |
| C.在FeCl3溶液中加入铁粉防止氧化变质 |
| D.加入催化剂有利于SO2与O2反应制SO3 |
对于在一定条件下进行的化学反应:2SO2 + O2  2SO3 ,改变下列条件,可以提高反应物中的活化分子百分数的是
2SO3 ,改变下列条件,可以提高反应物中的活化分子百分数的是
| A.降低温度 | B.增大压强 | C.使用催化剂 | D.增大反应物浓度 |
在一定温度下,向容积固定且不变的某密闭容器中充入a mol NO2,发生如下反应:
2NO2(g)  N2O4(g);ΔH < 0。达平衡后再向容器中充入a mol NO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
N2O4(g);ΔH < 0。达平衡后再向容器中充入a mol NO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
| A.平均相对分子质量增大 | B.NO2的转化率提高 |
| C.NO2的质量分数增大 | D.反应放出的总热量大于原来的2倍 |
一定温度下,将1molA和1molB气体充入2L恒容密闭容器,发生反应A(g)+ B(g) xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是
xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是
| A.反应方程式中的x=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量物质D |
| D.t1~t3间该反应的平衡常数均为4 |
从下列事实所得出的解释或结论正确的是
| 选项 | 实验事实 | 解释或结论 |
| A | 2N2O5(g) 4NO2(g)+O2(g) ΔH>0 4NO2(g)+O2(g) ΔH>0在室温下能自发进行 | 这是一个熵增的反应 |
| B | 压缩针筒内的NO2和N2O4混合气体, 颜色先变深后变浅 | 增大压强,平衡向生成N2O4的方向移动,新平衡比旧平衡压强小 |
| C | 锌与稀硫酸反应过程中,开始反应后速率逐渐增大 | 该反应是放热反应 |
| D | 已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动 | 反应物的浓度一定降低 |
决定化学反应速率快慢的根本因素是
| A.温度和压强 |
| B.反应物的浓度 |
| C.参加反应的各物质的性质 |
| D.催化剂的加入 |
 zC,达到平衡,试填写下列空白:
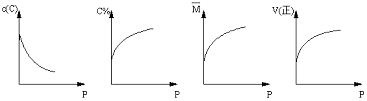
zC,达到平衡,试填写下列空白: xC(g),平衡后,C的体积分数为W%,若维持容器容积和温度不变,0.6molA 、0.3molB 和1.4molC为起始物质,达到平衡后,C的体积分数也为W% 。平衡后若缩小容器体积,C的浓度c(C)、C的体积分数C%、混合气体平均相对分子质量(M)和正反应速率[V(正)],随压强(P)的变化,一定符合的是
xC(g),平衡后,C的体积分数为W%,若维持容器容积和温度不变,0.6molA 、0.3molB 和1.4molC为起始物质,达到平衡后,C的体积分数也为W% 。平衡后若缩小容器体积,C的浓度c(C)、C的体积分数C%、混合气体平均相对分子质量(M)和正反应速率[V(正)],随压强(P)的变化,一定符合的是