题目内容
对于在一定条件下进行的化学反应:2SO2 + O2  2SO3 ,改变下列条件,可以提高反应物中的活化分子百分数的是
2SO3 ,改变下列条件,可以提高反应物中的活化分子百分数的是
| A.降低温度 | B.增大压强 | C.使用催化剂 | D.增大反应物浓度 |
C
解析试题分析:加入催化剂可提高反应物中的活化分子百分数;降低温度降低反应物中的活化分子百分数,而
压强和浓度只改变活化分子的数目,不改变百分数,故选C。
考点:活化能及其对化学反应速率的影响

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
以下各条件的改变可确认发生了化学平衡移动的是 ( )
| A.化学反应速率发生了改变 |
| B.有气态物质参加的可逆反应达到平衡后,改变了压强 |
| C.由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 |
| D.可逆反应达到平衡后,加入了催化剂 |
某兴趣小组为探究外界条件对可逆反应A(g)+B(g) C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的浓度为Ⅰ。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ。
C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的浓度为Ⅰ。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ。
针对上述系列实验,下列结论中错误的是( )
| | A | B | C |
| Ⅰ | 0.050mol·L-1 | 0.050mol·L-1 | 0.050mol·L-1 |
| Ⅱ | 0.070mol·L-1 | 0.070mol·L-1 | 0.098mol·L-1 |
| Ⅲ | 0.060mol·L-1 | 0.060mol·L-1 | 0.040mol·L-1 |
| Ⅳ | 0.080mol·L-1 | 0.080mol·L-1 | 0.12mol·L-1 |
A.由Ⅰ中数据可计算出该温度下反应的平衡常数K=20mol-1·L
B.Ⅱ可能是通过增大C的浓度实现的
C.若Ⅲ只是升高温度,则与Ⅰ比较,可以判断出正反应一定是放热反应
D.第Ⅳ组实验数据的得出,只能通过压缩容器的体积才可以实现
在4 L密闭容器中充入6 mol A气体和5 mol B气体,在一定条件下发生反应:
3A(g) + B(g)  2C(g) + xD(g) ,若平衡时生成了2 mol C,D的浓度为0.5 mol·L-1,下列判断正确的是( )
2C(g) + xD(g) ,若平衡时生成了2 mol C,D的浓度为0.5 mol·L-1,下列判断正确的是( )
| A.X=2 |
| B.平衡时混合气体密度增大 |
| C.平衡时B的浓度为1.5 mol·L-1 |
| D.当A与B的正反应速率为3:1时该反应达到平衡 |
化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是( )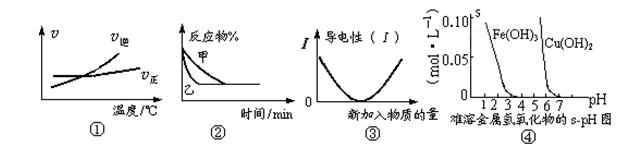
A.根据图①可判断可逆反应A2(g)+3B2(g) 2AB3(g)的ΔH>0 2AB3(g)的ΔH>0 |
B.图②表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.根据图④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO,至pH约为4 |
下列是工业上制取合成氨原料气氢气的一步重要反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0 ,该反应达到平衡后,为提高CO的转化率,下列措施中正确的是
| A.增大压强 | B.降低温度 | C.增大CO的浓度 | D.更换催化剂 |
下列变化过程中,ΔS<0的是 ( )
| A.氯化钠溶于水中 | B.NH3(g)和HCl(g)反应生成NH4Cl(s) |
| C.干冰的升华 | D.CaCO3(s)分解为CaO(s)和CO2(g) |
 C(g) + D(g)已达平衡状态:
C(g) + D(g)已达平衡状态: 2C(g)达到平衡标志的是
2C(g)达到平衡标志的是