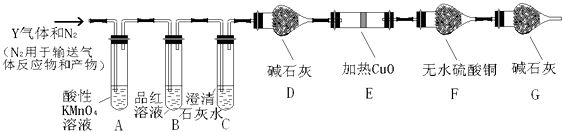
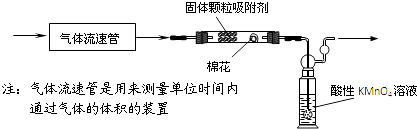
题目内容
【题目】实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.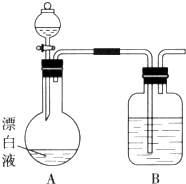
(1)小组同学依据漂白液具有漂白消毒的性质推测,漂白液中ClO﹣具有氧化性.实验如下:Ⅰ.用pH试纸检验,漂白液pH>7,饱和KAl(SO4)2溶液pH<7.
Ⅱ.取10mL漂白液,依次加入Na2SO3溶液和BaCl2溶液,有白色沉淀生成,经检验白色沉淀不溶于盐酸.
Ⅲ.另取10mL,漂白液,加入品红溶液,溶液红色逐渐变浅,一段时间后褪为无色.
Ⅳ.再取10mL漂白液,加入品红溶液,加入少量稀硫酸酸化后,溶液红色立即变为无色.
①漂白液pH大于7的原因是(用离子方程式表示) .
②由实验Ⅱ得出ClO﹣具有氧化性,写出反应的离子方程式 .
③对比实验Ⅲ和Ⅳ说明ClO﹣氧化性与溶液酸碱性的关系是 .
(2)小组同学依据(1)中的实验,提出:漂白液在酸性溶液中有Cl2生成.用如图所示的装置继续实验,探究漂白液在酸性溶液中是否能反应生成Cl2 . ①装置B的作用是 .
②若打开分液漏斗活塞向烧瓶中加入硫酸,不久烧瓶中有黄绿色气体产生.A中反应的离子方程式 .
③若打开分液漏斗活塞向烧瓶中加入饱和KAl(SO4)2溶液,首先观察到产生大量的白色胶状沉淀,不久烧瓶中有黄绿色气体产生.A中加KAl(SO4)2溶液反应的离子方程式是 .
(3)上述实验说明漂白液与酸性溶液混合会产生Cl2 . 若取10mL漂白液与足量BaCl2溶液混合后,不断通入SO2至过量,在实验过程中可能的实验现象是 .
【答案】
(1)ClO﹣+H2O?HClO+OH﹣;Ba2++ClO﹣+SO32﹣=BaSO4↓+Cl﹣;ClO﹣的氧化性随氢离子浓度增大而增大
(2)吸收氯气防止污染空气;ClO﹣+Cl﹣+2H+=Cl2↑+H2O;3ClO﹣+Al3++3H2O=3HClO+Al(OH)3↓
(3)生成白色沉淀
【解析】解:(1)①NaClO为强碱弱酸盐,水解显碱性,水解离子反应为ClO﹣+H2OHClO+OH﹣ , 所以答案是:ClO﹣+H2OHClO+OH﹣;②Ⅱ中由白色沉淀生成,经检验白色沉淀不溶于盐酸,可知白色沉淀为BaSO4 , 发生氧化还原反应,反应的离子方程式为:Ba2++ClO﹣+SO32﹣=BaSO4↓+Cl﹣;,
所以答案是:Ba2++ClO﹣+SO32﹣=BaSO4↓+Cl﹣;
③Ⅳ中加入少量稀硫酸酸化后,溶液红色立即变为无色,生成HClO,氧化性增强,
由上述两个实验对比可知,加入酸,反应速率加快,则ClO﹣的氧化性随氢离子浓度增大而增大,
所以答案是:ClO﹣的氧化性随氢离子浓度增大而增大;(2)①漂白液在酸性溶液中有Cl2生成,则分液漏斗中为酸,B中盛放NaOH溶液,其作用为吸收氯气、防止污染空气,
所以答案是:吸收氯气防止污染空气;
②次氯酸钙和氯化钙加入硫酸发生氧化还原反应生成氯气硫酸钙和水,反应的离子方程式为:ClO﹣+Cl﹣+2H+=Cl2↑+H2O,
所以答案是:ClO﹣+Cl﹣+2H+=Cl2↑+H2O;
③烧瓶中加入饱和KAl(SO4)2溶液,次氯酸根离子水解显碱性,铝离子水解显酸性,混合后水解相互促进,产生大量的白色胶状沉淀和次氯酸,反应的离子方程式为:
3ClO﹣+Al3++3H2O=3HClO+Al(OH)3↓,将烧瓶中的混合液在阳光照射下,不久烧瓶中有黄绿色气体产生为氯气,充分反应后集气瓶中收集到一种无色无味的气体为氧气.依据氧化还原反应电子守恒写出化学方程式配平得到:4HClO ![]() 2H2O+2Cl2↑+O2↑,
2H2O+2Cl2↑+O2↑,
所以答案是:3ClO﹣+Al3++3H2O=3HClO+Al(OH)3↓;(3)过量的SO2气体通入漂白液中,次氯酸具有氧化性氧化二氧化硫为硫酸,发生氧化还原反应,结合钡离子生成硫酸钡白色沉淀,
所以答案是:生成白色沉淀.

【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为 5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式___________________________________。增加压强,NO的转化率______________(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐______________ (填“增大”“不变”或“减小”)。
③由实验结果可知,脱硫反应速率______脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是________________。
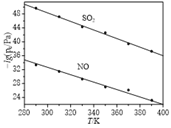
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压pc如图所示。由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均_________(填“增大”、“不变”或“减小”)。
【题目】对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图2: 
常温条件下的有关数据如表所示:
相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/gcm﹣3 | 颜色 | 水溶性 | |
对氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
对氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
对氯苯甲酸钾 | 194.5 | 具有盐的通性,属于可溶性盐 | ||||
实验步骤:在规格为250mL的装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g.
请回答下列问题:
(1)装置B的名称是 .
(2)量取6.00mL对氯甲苯应选用的仪器是 . (填选仪器序号).
A.10mL量筒
B.50mL容量瓶
C.50mL酸式滴定管
D.50mL碱式滴定管
(3)控制温度为93℃左右的方法是 . 对氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是 .
(4)第一次过滤的目的是 , 滤液中加入稀硫酸酸化,可观察到的实验现象是 .
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是 .
(6)本实验的产率是(填标号).
A.60%
B.70%
C.80%
D.90%