题目内容
【题目】下列说法不正确的是
A.1mol钠蒸气与2mol钠蒸气完全燃烧时,燃烧热相同
B.燃烧热是反应热的种类之一
C.在稀溶液中:H+(aq)+OH(aq)![]() H2O(l) ΔH=57.3kJ·mol1,若将含1molHNO3的稀溶液与含1molBa(OH)2的稀溶液混合,放出的热量为57.3kJ
H2O(l) ΔH=57.3kJ·mol1,若将含1molHNO3的稀溶液与含1molBa(OH)2的稀溶液混合,放出的热量为57.3kJ
D.在101kPa、25℃时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)![]() 2H2O(l) ΔH=+285.8kJ·mol1
2H2O(l) ΔH=+285.8kJ·mol1
【答案】D
【解析】
A.燃烧热是1mol可燃物完全燃烧放出的热量,1mol钠蒸气与2mol钠蒸气完全燃烧时,燃烧热相同,故A正确;
B. 燃烧热、中和热都是反应热的种类之一,故B正确;
C. 在稀溶液中:H+(aq)+OH(aq)![]() H2O(l) ΔH=57.3kJ·mol1,若将含1molHNO3的稀溶液与含1molBa(OH)2的稀溶液混合生成1mol水,所以放出的热量为57.3kJ,故C正确;
H2O(l) ΔH=57.3kJ·mol1,若将含1molHNO3的稀溶液与含1molBa(OH)2的稀溶液混合生成1mol水,所以放出的热量为57.3kJ,故C正确;
D. 在101kPa、25℃时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为H2(g)+![]() O2(g)
O2(g)![]() H2O(l) ΔH=-285.8kJ·mol1,故D错误。
H2O(l) ΔH=-285.8kJ·mol1,故D错误。

【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备己略)
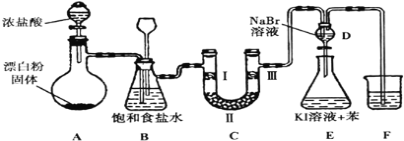
(1)装置A是氯气的发生装置,浓盐酸可与漂白粉的有效成分反应生成氯气。请写出相应反应的化学方程式:__________________________________;装置A部分用来装漂白粉的仪器名称是____________。
(2)装置B中饱和食盐水的作用是___________________________,同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞。请写出C中发生堵塞时B中的现象_________ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是___________(填字母编号).
编号 | Ⅰ | Ⅱ | Ⅲ |
a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)设计装置D、E的目的验证氧化性强弱顺序:Cl2 >Br2 >I2。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是_____________________,该现象______(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是________________。
(5)装置F的作用是___________,其烧杯中的溶液不能选用下列中的____________(填字母编号)。
a.饱和NaOH溶液 b.饱和NaCl溶液
c.饱和Na2SO3溶液 d.饱和Na2CO3溶液.