题目内容
【题目】下列说法正确的是
A.已知2C+SiO2![]() Si+2CO↑,说明Si的非金属性比C强
Si+2CO↑,说明Si的非金属性比C强
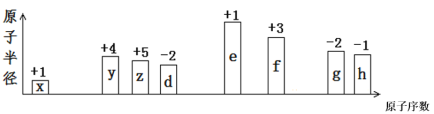
B.电子层数越多,原子半径一定越大
C.碱金属元素都能与氧气反应生成过氧化物
D.单质中不可能含有离子键
【答案】D
【解析】
A.反应中碳元素化合价升高被氧化,表现还原性,而比较非金属性利用的是单质的氧化性,所以该反应不能说明硅的非金属性比碳强,A选项错误;
B.原子核对核外电子的吸引,核外电子多,相应的核内质子数也多,静电作用力增强影响原子的半径,电子层数多少只是影响原子半径的因素之一,原子电子层数越多,对应的原子半径不一定大,如K比I少一电子层,但半径K比I大,B选项错误;
C.Li与氧气反应生成Li2O,不能生成过氧化物,C选项错误;
D.离子键是阴阳离子之间的静电作用,只存在于化合物中,单质中不可能存在离子键,D选项正确;
答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目