题目内容
11.下列关于如图所示电化学装置的分析正确的是( )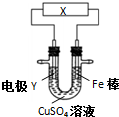
| A. | 若X为直流电源,Y为铜棒接正极,则Fe棒上镀铜 | |
| B. | 若X为直流电源,Y为碳棒接负极,则Fe棒被保护 | |
| C. | 若X为电流计,Y为锌棒,则SO42- 移向Fe棒 | |
| D. | 若X为导线,Y为铜棒,则Fe棒发生还原反应 |
分析 A、若X为直流电源,装置为电解池,接正极的为阳极,发生氧化反应;
B、若X为直流电源,装置为电解池,接正极的为阳极,发生氧化反应;
C、若X为电流计,装置为原电池,活泼金属作负极;
D、若X为导线,装置为原电池,活泼金属作负极,发生氧化反应.
解答 解:A、若X为直流电源,装置为电解池,Y为铜棒接正极,电解质溶液为硫酸铜溶液,为电镀池,Fe棒上镀铜,故A正确;
B、若X为直流电源,装置为电解池,Fe接正极的为阳极,发生氧化反应被腐蚀,故B错误;
C、若X为电流计,装置为原电池,活泼金属Zn作负极,阴离子SO42- 移向负极Zn,故C错误;
D、若X为导线,装置为原电池,活泼金属Fe作负极,Fe棒发生氧化反应,故D错误;
故选A.
点评 本题考查了电解池和原电池的反应原理,注意分清原电池、电解池、电镀池的区别和联系,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.某阴离子X2-有m个电子,其质量数为a,则核内中子数为( )
| A. | m+2 | B. | m+5 | C. | a-m+2 | D. | a-m-2 |
6.下表为元素周期表的一部分,列出10种元素在周期表中的位置.用化学符号回答下列问题:
(1)10种元素中,化学性质最活泼的金属是K.
(2)④、⑤、⑥三种元素最高价氧化物对应的水化物中,碱性最强的是NaOH.
(3)③、④三种元素形成的离子,离子半径由大到小的顺序是r(F-)>r(Na+).
(4)④和⑨两种元素形成化合物的化学式为NaBr,该化合物燃烧时的焰色为黄色,
该化合物溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=2Cl-+Br2.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑩ | ⑨ |
(2)④、⑤、⑥三种元素最高价氧化物对应的水化物中,碱性最强的是NaOH.
(3)③、④三种元素形成的离子,离子半径由大到小的顺序是r(F-)>r(Na+).
(4)④和⑨两种元素形成化合物的化学式为NaBr,该化合物燃烧时的焰色为黄色,
该化合物溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=2Cl-+Br2.
16.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol/L NaAlO2溶液中:H+、Na+、Cl-、SO3- | |
| B. | 无色溶液中:K+、Ca2+、Cl-、NO3- | |
| C. | 使酚酞变红色的溶液中:Na+、Cu2+、HCO3-、NO3- | |
| D. | 使石蕊变红的溶液中:H+、Na+、Fe2+、MnO4- |
20.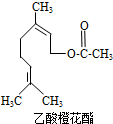 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,且属于芳香族化合物的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol.
 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,且属于芳香族化合物的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol.
| A. | ①②③ | B. | ①②⑤ | C. | ①②⑤⑥ | D. | ③④⑥ |
1.下列有机物命名正确的是( )
| A. | 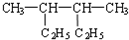 2,3-二乙基丁烷 | B. | 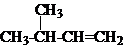 2-甲基-3-丁烯 | C. | 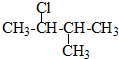 3-甲基-2-氯丁烷 | D. | 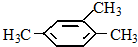 1,3,4-三甲苯 |


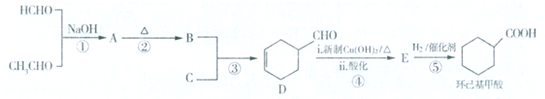
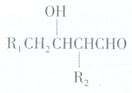 或
或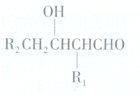
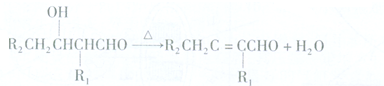
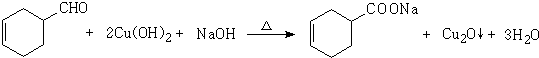 .
.